下列图示与对应的叙述不相符的是
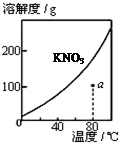
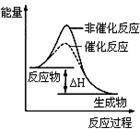
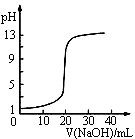

图1 图2 图3 图4
| A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C.图3表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1醋酸溶液得到的滴定曲线 |
| D.图4是亚硫酸氢钠粉末投入稀硝酸溶液中有关图像 |
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积的关系如图所示。则原H2SO4物质的量浓度是
| A.1mol/L | B.2mol/L | C.3mol/L | D.4mol/L |
在120℃和常压下,向100mL CH4和N2的混合气体中通入300mL O2,点燃使其完全反应,最后用足量的过氧化钠固体充分吸收,在相同条件下得到干燥气体340mL,则反应前混合气体中CH4和N2的物质的量之比为
| A.1:4 | B.1:1 | C.1:2 | D.2:3 |
零排放燃料电池曾被美国《时代》杂志列为21世纪改变人类生活的十大新科技之首。其中最具代表意义的质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极。下列说法中不正确的是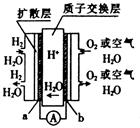
| A.a极为该电池的负极 |
| B.该电池的正极反应式为O2 + 4H+ + 4e-=2H2O |
| C.该电池的能量转化主要形式是化学能转化为电能 |
| D.H+(质子)由正极移动至负极 |
一定质量的铁和铜的混合物,与一定浓度的硝酸反应后容器中没有固体剩余,生成标准状况下2.24LNO和4.48LNO2(不考虑N2O4的存在)的混合气体,则参加反应的HNO3的物质的量是
| A.0.5 mol | B.0.8 mol | C.1.0 mol | D.1.6 mol |
测知氯化钠晶体中相邻的Na+离子与Cl-离子的距离为a cm,该晶体密度为ρg/cm3,则阿伏加德罗常数可表示为
| A.0.585/4a3ρ | B.58.5/8a3ρ | C.58.5/2a3ρ | D.117/a3ρ |