下列离子方程式与所述事实相符且正确的是
| A.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=== 4Fe3++6Cl-+Br2 |
| B.磁性氧化铁溶于氢碘酸:Fe3O4+8H+=== 2Fe3++Fe2++4H2O |
| C.放置在空气中的淀粉碘化钾溶液一段时间后溶液呈蓝色:4H++4I-+O2===2I2+2H2O |
| D.向硝酸铵溶液中滴加NaOH溶液:NH4++OH-=== NH3↑+ H2O |
常温下,下列溶液中一定能大量共存的离子组是
| A.使pH试纸呈红色的溶液:Na+、[Al(OH)4]-、SO42-、Cl- |
| B.澄清透明溶液:Cr2O72–、SO42–、K+、NO3– |
| C.pH=0的溶液:Na+、C2O42–、Fe3+、NO2– |
| D.水电离产生的c(H+)=1×10–12 mol·L–1的溶液:HCO3–、NH4+、Cl–、Ca2+ |
下列说法不正确的是
| A.溶液、胶体和悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 |
| B.仅用新制的氢氧化铜悬浊液一种试剂可鉴别乙醇、甘油、乙醛、乙酸、乙酸乙酯、葡萄糖溶液(必要时可加热) |
| C.过氧化氢在酶催化作用下的分解反应速率随温度的变化关系如下图Ⅰ所示 |
| D.在实验室中从苯酚中分离出苯,可选用的操作、装置如下图Ⅱ所示 |

设NA表示阿伏加德罗常数的值,下列叙述不正确的是
| A.标准状况下,11.2 L三氯甲烷所含分子数为0.5NA |
| B.常温常压下,1 mol甲基(?CH3)所含电子数为9NA |
| C.常温常压下,22 g氧气和26 g臭氧混合后,混合气体所含氧原子总数为3NA |
D.标准状况下,将22.4 L的NO2通入足量水中发生反应,转移的电子总数为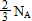 |
化学与生产、生活、社会密切相关。下列有关说法中不正确的是
A.日本福岛第一核电站核泄漏的具有放射性的 I、 I、 Cs可能持续影响数十年。其中 Cs可能持续影响数十年。其中 I的中子数比 I的中子数比 Cs的中子数少1 Cs的中子数少1 |
| B.我国部分城市已陆续开始推广使用“甲醇汽油”。“甲醇汽油”具有降低排放、节省石油、安全方便等特点。 |
| C.“反式脂肪酸”对人类健康危害极大,它的形成是由于油脂氢化过程中双键的顺式结构转变成室温下更稳定的固态反式结构 |
| D.废弃的塑料、金属、纸制品是可回收利用的资源,而玻璃是不可回收再利用 |
关于常温下pH=3的醋酸溶液,下列叙述正确的是
| A.加水稀释10倍后,pH=4 |
| B.加水稀释后,溶液中c(H+)和c(OH-)均减少 |
| C.加入醋酸钠晶体后,溶液的pH增大 |
| D.加入等体积、pH=11的NaOH溶液后,c(Na+)= c(CH3COO-) |