密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是
A. A、B两点表示在某时刻达到平衡状态,此时A、B两点时容器中,n(A)总∶n(B)总= 4∶5
B. A、C两点都表示达到平衡状态,则自反应开始到达平衡状态所需的时间tA<tC
C. 设B、C两点的平衡常数分别为KB、KC,则KB<KC
D. 在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率
在由水电离出的c(H+)=10-13mol·L-1的溶液中一定能够大量存在的离子组是
| A.Ba2+、Na+、Cl-、NO3- | B.Al3+、Ca2+、SO42-、Br- |
| C.NH4+、K+、HSO3-、CO32- | D.Na+、K+、Cl-、I- |
已知某镍镉(Ni-Cd) 可充电电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O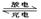 Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
| A.放电时Cd电极发生氧化反应 |
| B.放电时电解质溶液中的OH-向负极移动 |
| C.放电时负极附近溶液的碱性不变 |
| D.充电时阳极反应:Ni(OH)2+OH—+e—=NiOOH+H2O |
下列实验基本操作正确的是
| A.酸式滴定管洗净后直接装待装液 |
| B.用玻璃棒蘸取溶液滴到湿润的pH试纸上测其pH |
| C.用碱式滴定管量取0.10 mol·L-1的Na2CO3溶液22.10 mL |
| D.配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
将0.1 L含有0.02mol CuSO4和0.01mol NaCl的水溶液用惰性电极电解。电解一段时间后,一个电极上得到0.01 mol Cu,另一电极析出的气体
| A.只有Cl2 | B.只有O2 | C.只有H2 | D.既有Cl2又有O2 |
在常温下,pH=3的盐酸与pH=11的某一元碱等体积混合,所得溶液的pH
| A.等于7 | B.小于或等于7 | C.大于或等于7 | D.无法确定 |