已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-2b kJ·mol—1 |
| B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l);ΔH=2b kJ·mol—1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-4b kJ·mol—1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=b kJ·mol—1 |
化学实验应与化工生产一样遵循绿色化学的原则,实现原料和过程绿色化。下列操作符合绿色化学原则的是
| A.为便于观察铜在氯气中燃烧的现象,加大氯气的使用量 |
| B.实验室改用H2O2和MnO2反应,代替加热KClO3和MnO2制取氧气 |
| C.焚烧塑料、橡胶等废弃物是处理城市生产、生活垃圾的有效方法 |
D.制取CuSO4: Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O |
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为: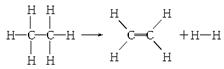
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是( )
| A.该反应放出251.2 kJ的热量 | B.该反应吸收251.2 kJ的热量 |
| C.该反应放出125.6 kJ的热量 | D.该反应吸收125.6 kJ的热量 |
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
| A.它是副族元素 | B.它是第六周期元素 |
| C.它的原子核内有63个质子 | D.它的一种同位素的核内有89个中子 |
氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO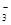 +3HSO
+3HSO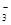 ===3SO
===3SO +Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。下图为用ClO
+Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。下图为用ClO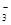 在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )
在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )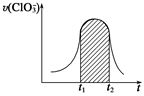
| A.反应开始时速率增大可能是c(H+)增大引起的 |
| B.纵坐标为v(H+)的速率—时间曲线与图中曲线能完全重合 |
| C.后期反应速率下降的主要原因是反应物的浓度减小 |
D.图中的阴影部分“面积”为t1~t2时间内ClO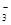 的物质的量浓度的减小值 的物质的量浓度的减小值 |
燃料电池是燃料(如H2、CO、CH4等)跟氧气或空气起反应,将化学能转变为电能的装置,电解液为强碱溶液。下列关于甲烷燃料电池的说法正确的是()
| A.负极反应为CH4+10OH-→CO32-+7H2O+8e- |
| B.负极反应为O2+2H2O+4e-→4OH- |
| C.随着放电进行,溶液中的阳离子向负极移动 |
| D.随着放电进行,溶液的PH不变 |