某化学兴趣小组利用以下装置探究气体的制取及性质。结合下图回答有关问题:

请结合图示实验装置,回答下列问题。
(1)用加热高锰酸钾制氧气选用发生装置是 ;该反应的符号表达式为
若用装置G收集氧气,氧气应从 端通入(选填“a”或“b”),用此装置收集氧气时检验氧气收集满的方法
(2)已知CO2能溶于水且与能水反应,密度比空气大,实验室可用块状大理石和稀盐酸来制取CO2,可选用的装置组合是 ,若用F装置收集CO2,油层的作用是 。
(3)小明同学选用如图所示的装置制取氧气。制取过程中所发生的符号表达式为: 实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现。该实验操作的目的是 。

(4)小红同学通过互联网得知:CuSO4溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解。
【初次探究】实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解,如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后
【再次探究】CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用。小红同学作了以下分析和设计。
①小红同学认为最不可能的是H2O,他的理由是 。
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动。
| 实验步骤 |
实验现象 |
结论 |
| a. 取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 |
溶液几乎没有气泡放出 |
实验证明,起催化作用的是 |
| B. 另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴氯化铜溶液[来 |
溶液中有大量气泡放出 |
(5).小玲同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,该同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想 I:反应生成的二氧化锰分解放出O2;
猜想Ⅱ:反应生成的锰酸钾分解放出O2;
猜想Ⅲ:
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想______错误;
第二组同学取高锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是__ ____.
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快。请说明高锰酸钾在氯酸钾的分解反应中是否作催化剂,为什么?
某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”感到非常好奇,设计实验进行探究。
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【查阅资料】① 人呼出的气体中主要成分是N2、O2、CO2和水蒸气等。
② 二氧化碳能与氢氧化钠发生反应,生成可溶性的碳酸钠和水。该反应的化学方程式是___。
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
(1)实验操作如右图所示。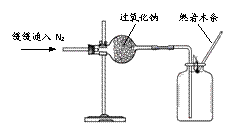
(2)实验现象及结论:观察到________现象,判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。其中A装置的作用是______,试管中发生的变化是______ 变化(填“物理”或“化学” )。
A B C
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。
(2)实验记录
| 实验操作 |
主要实验现象 |
实验结论及解释 |
|
| ① |
检查装置的气密性。 向装置中加入药品。 |
|
装置的气密性良好。 |
| ② |
打开分液漏斗的活塞,向A装置中缓慢加入稀盐酸。 |
______________ |
A装置中发生反应的化学方程式为__________; C装置作用是________。 |
| ③ |
一段时间后用带火星的木条在D内进行检验。 |
带火星的木条复燃。 |
过氧化钠与二氧化碳反应并生成氧气。 |
【实验反思】
(1)根据实验Ⅱ,过氧化钠与水蒸气反应后,还产生了另一种物质,该物质是_____(填“单质”或“化合物”)。
(2)若实验Ⅲ中过氧化钠和二氧化碳反应时生成碳酸钠和氧气,该反应的化学方程式是___。某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是______。
某小组同学做“硫在氧气中燃烧”的实验时,老师建议在集气瓶底部放少量NaOH溶液吸收生成的SO2。这种做法引起了同学们的思考:SO2与NaOH是否发生反应。
【查阅资料】通常状况下,1体积水约能溶解40体积SO2。
【实验方案】同学们向充满SO2的软塑料瓶中倒入一定量NaOH溶液,拧紧瓶盖,振荡,发现塑料瓶变瘪,他们认为SO2与NaOH发生了反应。
【反思与改进】甲同学认为上述实验不够严谨,理由是____________________。于是同学们设计了如下两个改进方案。
方案一
| 实验操作 |
实验现象 |
| 向两个充满SO2的200 mL软塑料瓶中分别注入10 mL的水和NaOH溶液,振荡、对比。 |
两个瓶子变瘪的程度 完全相同 |
乙同学认为由于两个瓶子变瘪的程度完全相同,因此无法证明SO2与NaOH是否发生了反应。试分析导致两个瓶子变瘪的程度完全相同的原因是_________________________________。他认为若改变注入水和NaOH溶液的体积便可达到实验目的,注入液体的体积可以是____(填序号)。
a.15 mL b.8 mL c.5 mL d.3 Ml
方案二
| 实验操作 |
实验现象 |
利用右图所示装置分别进行实验:向两个充满SO2的300 mL集气瓶中分别加入6 mL水和NaOH溶液,一段时间后,打开止水夹,对比。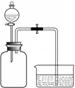 |
倒吸入两个集气瓶中 的液体体积完全相同。 |
丙同学认为上述方案也无法证明SO2与NaOH是否发生反应。
你认为导致吸入液体的体积完全相同的原因是_________________________________。
丁同学思考后,将上述装置进行了改进,便可达到实验目的。
改进装置如下图所示,你认为装置B的作用是_________________________________。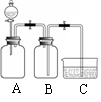
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将x g KClO3与1.0 g MnO2均匀混合加热
Ⅱ.将3.0 g KClO3与1.0 g CuO均匀混合加热在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中x的值应为________;Ⅱ中反应的化学方程式是________。
(2)乙探究了影响双氧水分解速度的某种因素。实验数据记录如下:
| |
双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2的体积 |
| Ⅰ |
50.0 g |
1% |
0.1 g |
9 mL |
| Ⅱ |
50.0 g |
2% |
0.1 g |
16 mL |
| Ⅲ |
50.0 g |
4% |
0.1 g |
31 mL |
本实验中,测量O2的体积可选用下图中的______(填字母序号)。
A B C D
实验结论:在相同条件下,___________。丙用右图装置进行实验,通过比较__________也能达到实验目的。
类比法是化学研究物质的重要方法之一。草酸的化学性质与碳酸相似。已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物。某校研究性学习小组对此展开探究:
⑴ 小明首先根据草酸中含有 元素,可推测生成物中含有水。
⑵ 小明对分解生成的其他产物进行猜测、验证:
【假设一】生成物中有二氧化碳
实验一:将生成的气体通入澄清的石灰水,实验现象是 ,小明据此判断生成物中含有二氧化碳。
【假设二】生成物中有一氧化碳
实验二:小明用右图装置进行实验,从而证明生成物中含有一氧化碳。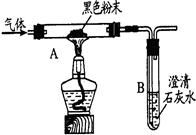
请回答:A装置中黑色固体粉末是 (填化学式),
A装置中的实验现象是 。
⑶ 讨论交流:小芳认为,小明的“实验二”不需要B装置也能够推断出生成物中含有一氧化碳,你是否支持小芳的观点: (填“支持”或“不支持”),请说出你的理由: 。小芳认为,从环保的角度看,“实验二”装置有一个缺陷,请你指出该缺陷: ,处理的方法是 。
小芳将一氧化碳通入铜和氧化铜混合粉末共10克的试管中,加热至黑色粉末全部转变成红色后,冷却,称得试管中铜粉为9克,求原混合物中氧化铜的质量分数。(写出计算过程)
如图是为探究物质燃烧条件设计的实验.甲中的白磷未燃烧,而乙中的白磷发生了燃烧.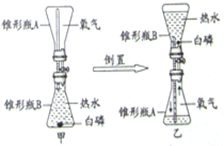
(1)该实验主要探究的燃烧条件是;
(2)白磷(P4)燃烧的产物与红磷相同,请写出白磷燃烧的化学方程式:;
(3)如仅用该装置进行实验,验证空气中氧气的体积分数约为 ,应做到:①白磷;②将锥形瓶B。