2011年4月台湾曝出的增塑剂风波一度让人们“谈塑色变”。常用的增塑剂如下:
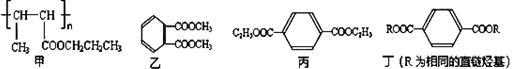
请回答下列问题:
(1)下列对甲的叙述正确的是 (填选项字母)
| A.甲能使Br2的CCl4溶液退色 |
| B.甲的单体是CH3CH = CHCOOCH2CH2CH3 |
| C.1 mol甲能与1 mol NaOH发生水解反应 |
| D.甲能发生酯化反应、取代反应、消去反应、加成反应 |
(2)丙中含有的官能团名称是 。
(3)乙的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式 。
(4)已知通过燃烧法确定丁的含氧量(质量分数)为23%。以某烃A为原料合成该塑料增塑剂的流程如下:

①反应1的反应条件是 。
②反应2的反应类型是 。
③反应3的化学方程式是 。
下图中A~J分别代表相关反应的一种物质,图中有部分生成物未标出。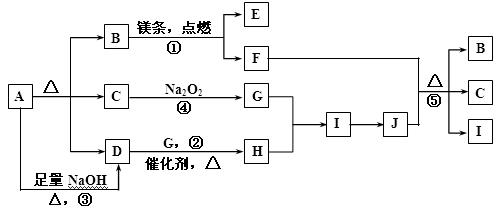
已知:A分解得到等物质的量的B、C、D;反应①为:2Mg+CO2 2MgO+C。
2MgO+C。
(1)A的化学式。
(2)写出反应②的化学方程式:。
(3)写出反应③的离子方程式:。
(4)写出反应⑤的化学方程式:。
(5)在反应④中,当生成标准状况下2.24 L G时,转移电子mol。
A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系: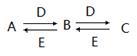
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,则A的化学式为,D的化学式为;A、C反应生成B的离子方程式为 。
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因_______________,C与E反应生成B的化学方程式为 。
【化学-选修5:有机化学基础】
用乙烯、甲苯、D三种原料合成高分子化合物J和有机中间体K的路线如下:
回答下列问题:
(1)C中官能团的名称是__________________,D的系统命名名称是__________________;
(2)K的结构简式是__________________;
(3)F→G的化学反应方程式是_______________________________;
(4)I→J属于加聚反应,J的结构简式是_________________;
(5)写出生成I的化学反应方程式______________________________;
(6)M与C互为同系物,质谱图显示其最大质荷比为136,符合下列条件的M的同分异构体有___________种。
①属于芳香族化合物②能发生银镜反应。
现有A-G七种物质,已知A是赤铁矿的主要成分,E是浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系。
(1)写出下列物质的化学式;E:,D:.
(2)在反应①②③中,属于置换反应的是 (填序号)。
(3)工业上常利用反应①的原理练铁,写出反应①的化学方程式。
(4)写出物质C与E的稀溶液发生反应的离子方程式:。
下图中每一个方格表示有关的一种反应物或生成物(部分的产物已省略);X加热产生A、B、C三种物质,其中A、C为无色气体,B在常温下是一种无色的液体;X与NaOH溶液在加热的条件下产生一种能使湿润的红色石蕊试纸变蓝的气体C;X与HCl反应产生一种无色无味的气体A,它能使澄清的石灰水变浑浊;请填下列空白:
(1)物质x可以是,B是,C是,F是。(填写化学式)
(2)反应①的化学方程式。
(3)F→G的化学方程式。