向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
已知0.1mol/L的碳酸氢钠溶液的pH为8.4,则下列说法正确的是
| A.加入少量NaOH固体,钠离子和碳酸根离子浓度均增大 |
B.将该溶液加水稀释,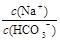 的比值保持不变 的比值保持不变 |
| C.c(Na+)+c(H+)=c(HCO3- )+c(CO32-)+c(OH-) |
| D.c(Na+)=c(HCO3- )+2c(CO32-)+c(H2CO3) |
氢叠氮酸(HN3)与醋酸的酸性相近,其盐稳定,但受撞击时会发生爆炸,生成氮气。关于把叠氮酸有以下说法:①NaN3水溶液呈碱性;②HN3固体属于分子晶体;③固体NaN3属于离子晶体;④NaN3可用于小汽车防撞保护气囊。其中正确的是
| A.①②③ | B.①②③④ | C.②③④ | D.①③④ |
已建立平衡的可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增加; ②生成物的产量一定增加;
③反应物的转化率一定增加; ④反应物物质的量浓度一定减小;
⑤正反应速率一定大于逆反应速率; ⑥使用了催化剂
| A.①② | B.②⑤ | C.③⑤ | D.③④⑥ |
已知反应:
①101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1下列结论正确的是
| A.碳的燃烧热大于110.5 kJ·mol-1 |
| B.①的反应热为 221 kJ·mol-1 |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
下列实验不能达到目的的是
A B C D
| A.测定一定时间内生成H2的反应速率 | B.用CO2的做喷泉实验 |
| C.验证NH3易溶于水 | D.比较Na2CO3和NaHCO3的热稳定性 |