“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解
④不能用电解熔融的AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
| A.①④ | B.②④ | C.①②④ | D.①②③④ |
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是
| 选项 |
W |
X |
| A |
盐酸 |
Na2CO3溶液 |
| B |
Cl2 |
Fe |
| C |
CO2 |
Ca(OH)2溶液 |
| D |
NaOH溶液 |
AlCl3溶液 |
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有
| A.15 | B.28 | C.32 | D.40 |
氯原子对O3的分解有催化作用:
O3+Cl==ClO+O2ΔH1,ClO+O ="=" Cl+O2ΔH2。大气臭氧层的分解反应是:O3+O ="==" 2O2ΔH,该反应的能量变化如图所示,则下列叙述正确的是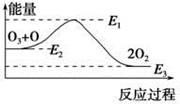
| A.反应O3+O ="==" 2O2的ΔH = E1-E3 |
| B.反应O3+O ="==" 2O2是吸热反应 |
| C.ΔH = ΔH1+ΔH2 |
| D.氯原子没有改变O3分解反应的历程 |
用氯气制取并获得碘单质,不能实现实验目的的装置是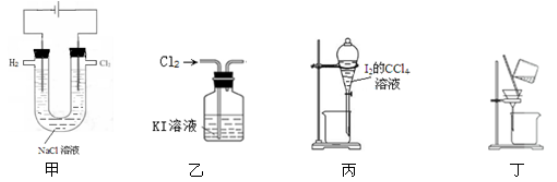
| A.用甲制取少量氯气 | B.用乙氧化溶液中的碘离子 |
| C.用丙提取置换出来的碘 | D.用丁过滤I2的CCl4溶液得碘单质 |
依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是
| A.卤素单质Cl2、Br2、I2的氧化性强弱 |
| B.气态氢化物NH3、H2O、HF的稳定性 |
| C.碱金属单质Li、Na、K与水反应的剧烈程度 |
| D.1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少 |