下列物质转化在给定条件下不能实现的是
①Si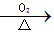 SiO2
SiO2 H2SiO3
H2SiO3
②S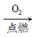 SO3
SO3 H2SO4
H2SO4
③C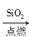 CO2
CO2 Na2CO3
Na2CO3
④MgCl2溶液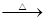 MgCl2·6H2O
MgCl2·6H2O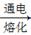 Mg
Mg
⑤Na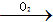 Na2O2
Na2O2 NaOH
NaOH
| A.①②③ | B.①②④ | C.①②③④ | D.①②③④⑤ |
下列反应中必须加入还原剂才能进行的是
| A.CuO→CuCl2 | B.Zn→ Zn2+ | C.H2→H2O | D.Cl2→Cl- |
某10% NaOH溶液,加热蒸发掉100g水后得到80mL20%的溶液,则该20% NaOH溶液的物质的量浓度为
| A.6.25mol/L | B.12.5mol/L | C.7mol/L | D.7.5mol/L |
将17克气体H2A通入水中形成500ml溶液,完全中和该二元酸用去NaOH 40克,则下列说法正确的是
A.该气体的摩尔质量为34 |
B.17克该气体物质的量为0.5mol |
| C.标况下该气体的摩尔体积为22.4升 | D.500ml溶液物质的量浓度为2mol/L |
有五瓶溶液分别是①10毫升0.60摩/升NaOH水溶液②20毫升0.50摩/升硫酸水溶液③30毫升0.40摩/升HCl溶液④40毫升0.30摩/升CH3COOH水溶液⑤50毫升0.20摩/升蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
| A.①>②>③>④>⑤ | B.②>①>③>④>⑤ |
| C.②>③>④>①>⑤ | D.⑤>④>③>②>① |
下列仪器在使用之前需要检查是否漏液的是
①分液漏斗②容量瓶③长颈漏斗④普通漏斗
| A.①② | B.①②③ | C.②③④ | D.①②③④ |