某强酸性溶液X,含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、NO3-中的一种或几种离子,取溶液进行连续实验,能实现如下转化: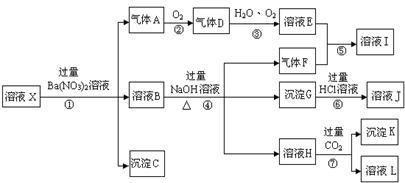
依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是:________________;不能肯定的是:_______________。对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中,根据现象就可判断,则该试剂是:_________。(选填:①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸,⑤KSCN溶液,⑥KMnO4溶液)
(2)气体F的电子式为:_______________,实验中,可以观察到反应②的现象是:__________________。
(3)写出步骤①所有发生反应的离子方程式________________________、___________________。
醋酸乙烯酯是制备聚乙烯醇的原料,用途广泛。某种制备醋酸乙烯酯的流程如下: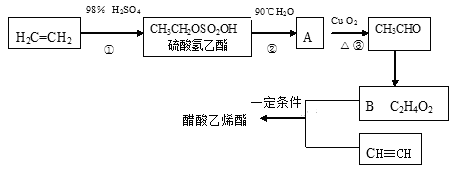
(1)醋酸乙烯酯中官能团的名称:_________________;反应类型:①______________,②________________.
(2)HO—CH2—CHO的名称(系统命名)是_____________________________.
(3)写出反应③的方程式:___________________________________________________.
(4)写出符合下列要求的醋酸乙烯酯的同分异构体的结构简式:____________________.
①分子中含有环的结构
②1mol该物质与足量的金属钠反应产生1mol气体。
③核磁共振氢谱只显示3个吸收峰且峰的高度相同
(5)下列说法不正确的是()
a.实验室制取乙烯采取水浴加热
b.硫酸氢乙酯可以与氨气反应生成盐
c.乙炔中含有的乙烯杂质可以通过酸性高锰酸钾除去
d.A和B都含有π键
[化学一选修5:有机化学基础](15分)环己基甲酸是一种无色或浅黄色油状液体,环己基甲酸及其衍生物是重要的有机化工原料和合成药物的中间体,在新材料和药物研发中具有广泛的价值。其合成方法如下: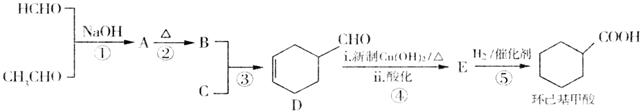
其中链烃C的相对分子质量在50~70之间,碳氢原子个数比为2:3,核磁共振氢谱显示有两个峰且面积比为2:l。回答下列问题:
已知: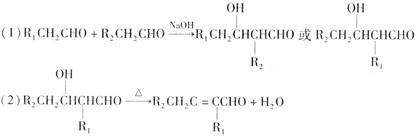
(1)C的结构简式为,其化学名称为。
(2)A的结构简式为。
(3)写出下列反应的反应类型:②;⑤。
(4)写出D与新制Cu(OH)2反应的化学方程式。
(5)若反应④、⑤的顺序交换是否可行(填“是”或“否”),原因是。
(6)符合下列条件的环己基甲酸的同分异构体有种。
①含有六元碳环 ②能发生银镜反应 ③不考虑立体异构
Atropic酸(H)是某些具有消炎、镇痛作用药物的中间体,其一种合成路线如下: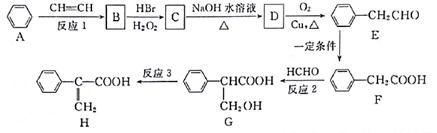
(1)G中含氧官能团的名称是________;反应1为如成反应,则B的结构简式是。
(2)C→D的化学方程式是。
(3)反应2的反应类型为,反应3的反应条件为____。
(4)下列说法正确的是 。
a.B中所有原子可能在同一平面上
b.合成路线中所涉及的有机物均为芳香族化合物
c.一定条件下1 mol有机物H最多能与5 mol H2发生反应
d.G能发生取代、加成、消去、氧化、缩聚等反应
(5)化合物G有多种同分异构体,其中同时满足下列条件:
①能发生水解反应和银镜反应;
②能与FeCl3发生显色反应;
③核磁共振氢谱只有4个吸收峰的同分异构体的结构简式是__。
有机化学反应在因反应条件不同,可生成不同的有机产品。例如: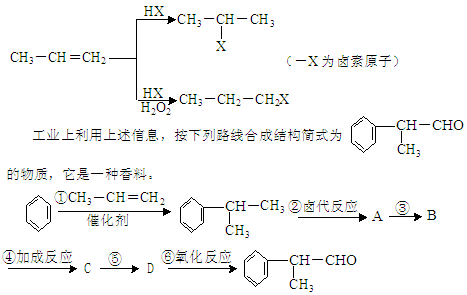
请根据上述路线,回答下列问题:
(1)A的结构简式可能为_____________________________________。
(2)反应①、③、⑤的反应类型分别为_______、________、_________。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):_________________________
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是__________________________________________________________
(5)这种香料是具有多种同分异构体,其中某种物质有下列性质:
①该物质的水溶液遇FeCl3溶液呈紫色
②分子中有苯环,且苯环上的一溴代物有2种。
写出符合上述两条件的物质可能的结构简式(只写两种)_______________________________________。
德国化学家列培发现了一系列乙炔的高压反应(被称为列培反应),为有机合成工业作出了巨大的贡献。部分列培反应如下(条件从略):
a、HC≡CH + ROH → CH2=CHOR
b、HC≡CH + HCHO → HC≡CCH2OH
c、R2NCH2OH + HC≡CH → R2NCH2C≡CH + H2O
d、R2NH + HC≡CH → R2NCH =CH2
(1) 以上反应中属于加成反应的有(填序号)
(2)工业上可利用以上列培反应,以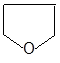 为原料合成高聚物
为原料合成高聚物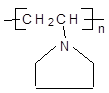 ,
,
反应流程如下: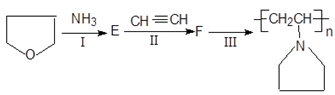
试完成下列问题:
①E的结构简式: 。
②写出反应I的反应类型 。
③写出反应Ⅲ的化学反应方程式。