一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g) 2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的
2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的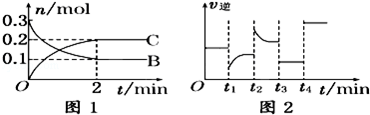
A.反应开始2分钟内,v(B)=0.05mol/(L•min)
B.t1时改变的条件可能是减小了反应物的浓度
C.t2时可能升高了温度,t3时改变的条件可能是降压,此时c(B)减小
D.T4时可能使用了催化剂
化学与生产、生活密切相关。下列有关叙述正确的是
| A.大气雾霾污染现象的产生与汽车尾气排放有关 |
| B.玻璃和氮化硅陶瓷都属于新型无机非金属材料 |
| C.空气中的臭氧对人体健康有益无害 |
| D.活性炭与二氧化硫都可用于漂白,其漂白原理相同 |
某澄清透明溶液中只可能含有:①A13+;②Mg2+;③Fe3+;④Cu2+;⑤H+;⑥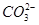 ;⑦
;⑦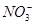 中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是
中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是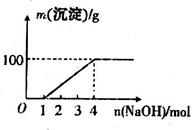
| A.②⑤⑦ | B.②⑤⑥ | C.③⑤⑦ | D.①④⑤ |
下图是某工厂对海水资源综合利用的示意图,下列说法错误的是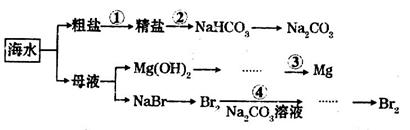
A.第①步中除去粗盐中的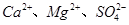 ,依次加入的物质可以是 ,依次加入的物质可以是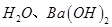 溶液、 溶液、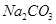 溶液和盐酸 溶液和盐酸 |
B.第②步发生的化学反应为: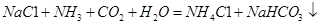 |
| C.第③步工业上电解熔融的Mg(OH)2冶炼金属Mg |
| D.第④步用Na2CO3溶液吸收Br2过程中,既有溴元素被氧化也有溴元素被还原 |
仅用下表提供的实验器材(夹持仪器和试剂任选),不能完成相应实验的是
下列各组微粒在指定环境中一定可大量共存的是
A. |
B.常温下,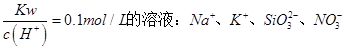 |
C.投入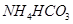 固体能产生气体的溶液: 固体能产生气体的溶液: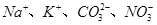 |
D.pH=1的溶液中: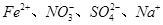 |