只有氧气才能支持燃烧吗?某学习小组对这个问题进行如下探究。
【信息给予】钠是一种银白色的金属,能与空气中的氧气与水蒸气反应。

【提出问题1】除氧气外,是否还有其他物质也能支持燃烧。
【进行实验一】如图,向盛有金属钠(Na)的硬质玻璃管中通入纯净、干燥的CO2,当观察到澄清石灰水中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,钠剧烈燃烧,产生白烟,燃烧结束后玻璃管中有黑色颗粒和白色固体生成。
【得出结论】二氧化碳 (1) (“能”或“不能”)支持某些物质燃烧。
【反思评价】点燃酒精灯前,要先向玻璃管中通会二氧化碳,其目的是____(2)__ 。
【提出问题2】黑色颗粒和白色固体是什么?
【猜想与假设】黑色颗粒可能是 (3) (用化学式填写)。
【进行实验二】现象:黑色颗粒逐渐减少,澄清石灰水______(4)____。
【得出结论】实验二证明:黑色颗粒的猜想是正确的。
【猜想与假设】某同学对白色固体的成分做出猜想:(Ⅰ)碳酸钠 (Ⅱ)氢氧化钠。你认为猜想 (5) (填序号)一定是错误的,理由是 (6) 。
【2015年山东省德州市】规范的操作是实验成功的基本保证。下面是有些同学的实验操作,请根据要求回答下列问题:
(1)A操作存在的错误是 ;
(2)B操作集气瓶中既无水又无细沙,可能造成的后果是 ;
(3)用C操作量取的水配制溶液的浓度比欲配制溶液 (填“偏大”或“偏小”);
(4)D操作可能造成的不良后果是 (写出一条即可)。
【2015年重庆市B】科学严谨的态度、安全规范的操作是成功进行化学实验的保障。
(1)化学实验安全第一,下列实验要特别注意安全的是 (填序号)。
A.取用大理石 B.称量粗盐 C.稀释浓硫酸 D.研碎胆矾
(2)根据下图,读出液体的体积为 mL ;精盐质量是 g 。
(3)实验室用下图所示的装处制取和收集某种气休,由装置可推知该气体的物理性质是 ,制取气体的反应一定是 (填序号)。
A.不需要加热
B.需要催化剂
C.制取氧气的反应
D.反应物都是固体
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,小强认为是该气体是 ,他的分析原因是 ,并用带火星的木条靠近P处检验证明了他的猜想.
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物.开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物应为Ca(OH)2.请解释小强否定原假设建立新假设的理由: 。
(3)请写出过氧化钙和水反应的化学方程式: 。
(4)小强在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论 。
(5)小强发现:CaO2与水反一段时间后,反应速度明显变慢,请猜想可能的原因: 。
(13)某校化学兴趣小组就空气中氧气的含量进行实验探究: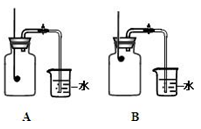
(1)小组同学设计了如右图所示的两套装置,你认为合理的是 (填字母)为了确保实验的成功,在装药品之前应该
(2)红磷在集气瓶中发生反应的文字表达式为 。该实验中红磷稍过量,目的是 。
(3)小组同学做完实验后发现水进入集气瓶的量远少于理论值.经讨论,同学们认为造成该现象的原因可能有_____________________或______________________
(4)若将红磷换成炭粉,该实验能否获得成功? ,理由是 。
(5)小淳同学对实验装置进行了大胆的改造,设计了如右图的装置。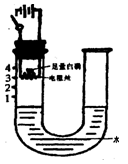
请根据图示回答下列问题:
①闭合电源开关,可以观察到白磷
②装置冷却到室温时,可观察到U型管内左侧液面
③通过这个实验得出的结论是
④此实验还可推知反应后剩余气体的两点性质是:
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】右下图是他们进行实验的装置图,气体发生装置中A仪器的名称是_____________,此实验中B处宜采用的气体收集方法是_______ _____。
【实验记录】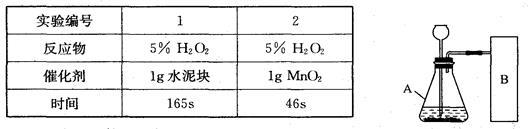
【结论】该探究过程得出的结论是_________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____ _____是否改变。
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
| 实验步骤 |
现象 |
结论 |
| 取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰。 |
缓慢有少量气泡冒出 |
|
| 另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰。 |
迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 |
现象 |
结论 |
| |
|
温度越高,过氧化氢分解的速率越大 |