将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气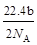 L L |
B.NA可表示为: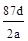 |
C.反应后溶液中的Cl―数目为: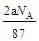 |
D.反应后溶液中的H+数目为: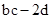 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理: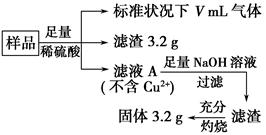
下列说法正确的是 ( )。
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B.样品中Fe元素的质量为2.24 g |
| C.样品中CuO的质量为4.0 g |
| D.V=896 mL |
下列推断正确的是( )。
| 事实 |
结论 |
|
| A |
常温下铁、铜均不溶于浓硫酸 |
常温下铁、铜与浓硫酸均不反应 |
| B |
HCl与Na2CO3溶液反应生成CO2 |
可用饱和Na2CO3溶液除去CO2中的少量HCl |
| C |
氧化铜高温下生成红色物质,该物质可与稀硫酸反应 |
氧化铜高温下可分解生成Cu2O |
| D |
稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 |
稀硝酸氧化性比浓硝酸强 |
美国“海狼”潜艇上的核反应堆内使用了液态铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是 ( )。
| A.原子半径:Na>Al |
| B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na) |
| C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 |
| D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成 |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是( )。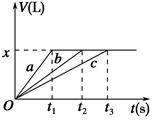
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
下列类比关系正确的是 ( )。
| A.钠与氧气在不同条件下反应会生成两种不同的氧化物,则Li与氧气反应也能生成Li2O或Li2O2 |
| B.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应可生成Na2SO3和O2 |
| C.Fe与Cl2反应生成FeCl3,则Fe与I2反应可生成FeI3 |
| D.Al与Fe2O3能发生铝热反应,则Al与MnO2也能发生铝热反应 |