有A、B、C、D四种物质,已知它们能发生下列变化:
①A2++B=B2++A ②A2++C=C2++A
③B2++C=C2++B ④C2++D=D2++C
由此可推知,各物质的氧化性、还原性强弱顺序正确的是
①氧化性:A2+>B2+>C2+>D2+
②氧化性:D2+>C2+>B2+>A2+
③还原性:A>B>C>D
④还原性:D>C>B>A
A.①③ B.①④ C.②④ D.②③
HPE是合成除草剂的重要中间体,其结构简式如下图所示。下列有关HPE的说法正确的是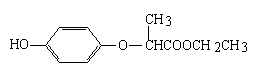
| A.HPE不能跟浓溴水反应 |
| B.1molHPE最多可以和2mol NaOH反应 |
| C.HPE在核磁共振氢谱中有6个峰 |
| D.HPE分子中有2个手性碳原子 |
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
| A.气态氢化物的稳定性:Z < Y < X | B.最高价氧化物水化物酸性:Z > Y |
| C.原子半径:Z < Y < X | D.元素非金属性:Z> Y > X |
氯气跟碘在加热条件下,以等物质的量进行反应,可得到一种红棕色液体ICl。ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式为:2ICl+2Zn===ZnCl2+ZnI2 ICl+H2O===HCl+HIO
下列叙述中正确的是
| A.ZnCl2既是氧化产物,又是还原产物 |
| B.ICl跟H2O的反应是自身氧化还原反应 |
| C.ZnI2既是氧化产物,又是还原产物 |
| D.在ICl跟H2O的反应中,ICl是氧化剂,H2O是还原剂 |
已知:NaA的水溶液呈碱性。常温下将等体积的0.10mol/L NaA溶液与0.05mol/L HCl溶液混合,所得溶液pH < 7。据此判断以下关系式不成立的是
A.c(Cl ̄) + c(OH ̄) + c(A ̄) > c(Na+ )
B.c(Na+ ) > c(A ̄) > c(H+ ) > c(OH ̄)
C.c(A ̄ ) + c(HA) = c(Na+ )
D.c(A ̄) > c(Na+ ) >c(H+ ) > c(OH ̄)
下列实验操作,正确的是
| A.中和滴定时,用标准液润洗滴定管,用待测液润洗锥形瓶,并滴入l mL指示剂 |
| B.配制物质的量浓度溶液时,将称量好的溶质溶于盛有适量水的烧杯中,溶解后立即倾入容量瓶中,继续进行洗涤和定容 |
| C.制取Fe(OH)2时,吸取NaOH溶液的胶头滴管的末端应插入FeSO4溶液中,再缓缓将NaOH溶液挤出 |
| D.溴乙烷和烧碱溶液共热后,将硝酸银溶液滴入水解液中,即可见到淡黄色沉淀 |