20℃时,将10 mL 0.1 mol/L Na2S2O3溶液和10 mL 0.1 mol/L的H2SO4溶液混合,2 min后溶液中明显出现浑浊。已知温度每升高10℃,化学反应速率增大到原来的2倍,那么50℃时,同样的反应要同样看到浑浊,需要的时间是
| A.40 s | B.15 s | C.48 s | D.20 s |
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钻(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为 ,下列说法正确的是()
,下列说法正确的是()
A.充电时,电池的负极反应为LiC6-e- Li+C6 Li+C6 |
B.放电时,电池的正极反应为CoO2+Li++e- LiCoO2 LiCoO2 |
| C.羧酸、醇等含活泼氢气的有机物可用作锂离子电池的电解质 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是()
| 选项 |
被提纯的物质(杂质) |
除杂试剂 |
分离方法 |
| A |
乙酸乙酯(乙酸) |
饱和碳酸钠溶液 |
分液 |
| B |
NH3(H2O) |
浓硫酸 |
洗气 |
| C |
KCl固体(I2) |
KOH溶液 |
加热 |
| D |
苯(苯酚) |
浓溴水 |
过滤 |
下列装置或操作能达到实验目的是()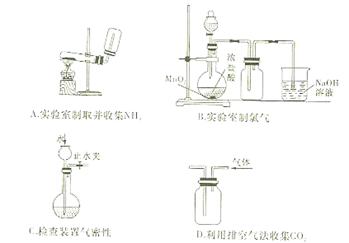
如图进行实验,试管内装有12mLNO,然后间歇而缓慢地通入8mLO2。下面有关实验最终状态的描述正确的是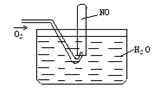
| A.试管内气体呈棕红色 | B.试管内气体为无色的NO |
| C.试管内气体为无色的O2 | D.试管内液面高度上升 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A.使红色布条褪色(HCl) |
| B.将NaHCO3固体加入新制氯水,有无色气泡(H+) |
| C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈血红色(Cl2) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |