已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大。其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、E的第一电离能由小到大的顺序为 。
(2)B的氯化物的熔点比D的氯化物的熔点 (填“高”或“低”)。
(3)氢化物A2H4分子中A原子采取 杂化。
(4)按原子的外围电子排布分区,元素F在 区,二价阳离子F2+与过量的A的简单氢化物的水溶液反应的离子方程式为 。
(5)元素A和C可形成一种新型化合物材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为 。
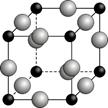
(6)A、F形成某种化合物的晶胞结构如右图所示的立方晶胞(其中A显-3价,每个球均表示1个原子),则其化学式为 。设阿伏伽德罗常数为NA,距离最近的两个F原子的核间距为a cm,则该化合物的晶胞密度为(用含a和NA的代数式表示) g/cm3。
主族元素A、B、C、D都是短周期元素,A、D同主族,B、C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体。它们在一定条 件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能剧烈反应生成A的单质。所得溶液中含有与氖原子的电子层结构相同的阳离子。
件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能剧烈反应生成A的单质。所得溶液中含有与氖原子的电子层结构相同的阳离子。
回答下列问题:(1)写出元素符号A____,B____,C____,D____。
(2)写出B单质与D在加热反应后生成物质的化学式___________ ___________。
___________。
写出符合下列条件的短周期元素.(提示:答案可能有多种) (6分)
①.最外层电子数是次外层电子数的1/2的元素.___________ (填元素符号,下同)
②.最外层有2个电子的元素_________________
③.M层电子数是L层电子数的3/4的元素_____________
将1mol/LNaOH溶液逐滴滴入盛有20 ml 1mol/LAlCl3溶液的试管中,边滴边振荡试管,能观察到的实验现象______________________________________,有关的化学方程式______________________________________________当加入_______mlNaOH沉淀达到最大值. (6分)
ml 1mol/LAlCl3溶液的试管中,边滴边振荡试管,能观察到的实验现象______________________________________,有关的化学方程式______________________________________________当加入_______mlNaOH沉淀达到最大值. (6分)
原子序数由小到大排列的四种短周期元素X、Y、Z、W,,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。四种元素的原子序数之和为32. (8分)
(1)则X是Y 是___________Z是____________(填元素符号)
(2)W在元 素周期表的位置是_______________________
素周期表的位置是_______________________
完成下反应的化学方程式或离子方程式(8分)
(1)铝与 氧化铁在高温下反应(铝热反应)
氧化铁在高温下反应(铝热反应)
______________________________________;
(2)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式
____________________________________________________________
(3)工业上用焦炭和二氧化硅反应制得粗硅(Si)
____________________________________________________________
(4)装氢氧化钠溶液的试剂瓶不用玻璃塞,原因用化学方程式表示为_________________________________________________________