核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:

(1)写出11号元素形成氧化物的化学式 。
(2)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体元素结尾。
(3)各写出一种核外电子排布与氖原子相同的离子符号:阳离子 、阴离子 。
(4)在第三周期中,各原子结构的共同之处是 ;该周期中,各原子核外电子排布的变化规律是 。
石油称为原油,没有固定的沸点。加热原油使其气化,再分别冷却,在不同温度下可分别得到汽油、柴油、沥青等石油产品,此过程称之为石油的分馏。将汽油、柴油等进一步高温加热,使其变成质量更小的气体分子——石油气,该过程叫石油的裂化。试回答:两过程中属于化学变化过程的是___________,原因是。
专家提醒:使用含氟牙膏的儿童,牙齿比较坚固,蛀牙少。你认为含氟牙膏比普通牙膏中多出的有利于儿童牙齿健康的化学元素是;但从保护臭氧层角度出发,环保专家大力提倡使用无空调、无冰箱等。可见,化学元素或化学物质既有有利的一面,也有不利的一面。请再举两例:
(1);(2)。
某学习小组完成“实验活动1氧气的实验室制取与性质”进行了研讨。请你参与完成下面的问题。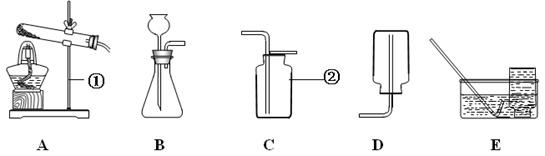
(1)写出图中指定仪器的名称:①_______________;②_______________。
(2)若选择装置A用高锰酸钾制取氧气,则试管口要放一团_______,该反应的文字表达式为_______________________________________;收集纯度高的氧气宜选用____(填序号,下同)。
(3)如果用双氧水、二氧化锰制氧气,则选用的发生装置是____;反应的文字表达式为________________________。
(4)用排空气法收集氧气,验满的方法是_________________________________________。
(5)F图是某同学加热氯酸钾制取氧气的装置,指出其中的错误__________________;要改正错误需要操作的按钮是_______(填字母)。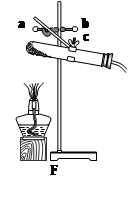
(6)实验操作:用高锰酸钾制取氧气的操作过程可概括为:“组装仪器→→装药品和放棉花并固定试管→加热试管→收集气体→将导管从水槽中取出→停止加热”。
(7)实验反思:在加热氯酸钾制取氧气的过程中,发现产生氧气的速率很慢,经检查不是氯酸钾变质,也不是装置气密性不好,你认为最可能的原因是。
实验时,我们需要熟悉一些实验的基本操作及操作过程需要注意的事项。
请你在题后横线上简要说明下列操作可能造成的不良后果:
(1)向燃着的酒精灯里添加酒精:____________。
(2)取细口瓶里的药液时,标签向下,没有向着手心:____________________。
(3)铁丝在氧气中燃烧,集气瓶中没有加少量的水或铺一层细沙:____________________。
(4)氧气收集完毕后,停止加热,没有从水中移出导管:__________________________。
“水是生命之源”。请回答下列与水有关的问题:
(1)鱼类可以在水中呼吸,是因为水中溶有______________;
(2)水体污染的来源主要有工业污染、农业污染、______________;
(3)蔗糖在热水中溶解比在冷水中快,用分子的相关知识解释:
_____________________________________________________;
温度升高,分子在水中的扩散速率加快,从而加速蔗糖溶解
(4)我国是世界人均水资源贫乏的国家之一.爱护水资源是我们的应尽义务.我们不仅要节约用水,同时还要防止水体污染.下列措施中不合理的是__________(填序号)。
① 生活中不使用含磷洗涤剂② 禁止施用农药化肥
③ 生活污水经净化后再排放④ 禁止在江河边倾倒垃圾
⑤ 抑制水中所有动、植物的生长⑥ 不任意排放工业废水
请举一例,说明你如何节约用水:_____________________________________。