用编号填空:
(1)下列关于燃烧热的说法正确的是
A.101kPa时1mol氢气完全燃烧生成水蒸气所放出的热量即氢气的燃烧热;
B.101kPa时1mol碳在氧气中燃烧生成CO所放出的热量即碳的燃烧热;
C.某物质的燃烧热不随热化学方程式计量数的改变而改变。
(2)下列关于用稀盐酸和氢氧化钠稀溶液测中和热的说法错误的是
A.实验结果随反应物用量改变而改变;
B.实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和;
C.实验中不可用环形铜质搅拌棒代替环形玻璃搅拌棒。
(3)下列关于化学平衡的说法错误的是
A.若改变影响化学平衡的条件之一,平衡向能够使这种改变减弱的方向移动;
B.达到化学平衡时,各组分的浓度不再改变,反应停止;
C.化学平衡移动,化学平衡常数不一定改变。
(4)改变下列条件,化学平衡一定向正反应方向移动的是
A.增大反应物浓度 B.升高温度 C.增大压强
(5)下列关于电解质的说法错误的是
A.酸、碱、盐及氧化物都是电解质;
B.电解质溶液能导电是因为发生了电离,产生了自由移动的离子;
C.电解质不一定能导电,能导电的物质不一定是电解质。
(6)下列反应的△H<0的是
A.铝和稀硫酸反应 B.碳酸氢铵受热分解 C.氢氧化钡晶体与氯化铵晶体反应
(7)下列情况,均为日常生活中为了改变反应速率而采取的措施,其中不属于浓度影响反应速率的是
A.汽车加大油门 B.食物放冰箱 C.糕点包装袋里放小包除氧剂
(8)下列实验现象与实际不符的是
A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊;
C.将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅。
(9)一定温度下,有三种酸:A.盐酸,B.硫酸,C.醋酸,回答下列问题:
①三种酸溶液等物质的量浓度时,c(H+)最大的是 ;
②三种酸的c(H+)相同时,溶液浓度最大的是 ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,再加入同样的锌粒,反应最快的是 。
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)目前常用的镍镉(Ni Cd)电池,其电池总反应可以表示为:
Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是( )
①以上反应是可逆反应
②以上反应不是可逆反应
③充电时化学能转变为电能
④放电时化学能转变为电能
| A.①③ | B.②④ | C.①④ | D.②③ |
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重。这是因为 。
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正极、负极,并写出电极反应。
正极反应 ;
负极反应 。
某兴趣小组为了提高电池的效率,设计了下图所示的原电池。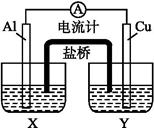
请回答下列问题:
(1)若X是AlCl3溶液,Y是稀硫酸,请你写出电极名称及电极反应:
Al片( ) ____________________________,
Cu片( ) ____________________________。
(2)若X是浓硝酸,Y是NaCl溶液,请你写出电极名称及电极反应:
Al片( ) ____________________________,
Cu片( ) ____________________________。
(1)事实证明,原电池中发生的反应通常是放热反应。利用下列化学反应可以设计成原电池的是 。
A.C(s)+H2O(g) CO(g)+H2(g) ΔH>0
CO(g)+H2(g) ΔH>0
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l) ΔH<0
NaCl(aq)+H2O(l) ΔH<0
C.2H2(g) +O2(g) 2H2O(l) ΔH<0
2H2O(l) ΔH<0
D.CaCO3(s)+2HCl(aq) CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
E.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH<0
CO2(g)+2H2O(l) ΔH<0
(2)有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等物质的量浓度的盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出。据此判断A、B、C、D的活动性由强到弱的顺序是 。
已知氨水与醋酸的电离程度在同温同浓度下相等,溶有一定量氨的氯化铵溶液呈碱性。现向少量的Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,固体完全溶解。
甲同学的解释是:
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)①
Mg2+(aq)+2OH-(aq)①
N+H2O NH3·H2O+H+②
NH3·H2O+H+②
H++OH- H2O③
H2O③
由于N水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是:
Mg(OH)2(s) Mg2+(aq)+2OH-(aq)①
Mg2+(aq)+2OH-(aq)①
N+OH- NH3·H2O②
NH3·H2O②
由于NH4Cl电离出的N与Mg(OH)2电离出的OH-结合,生成了弱电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学解释只有一种正确,他选用的试剂是 (填写编号)。
| A.NH4NO3 | B.CH3COONH4 |
| C.Na2CO3 | D.NH3·H2O |
(2)请你说明丙同学作出该选择的理由是 。
(3)丙同学将所选试剂滴入Mg(OH)2悬浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理 (填“甲”或“乙”);写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式 。