(1)事实证明,原电池中发生的反应通常是放热反应。利用下列化学反应可以设计成原电池的是 。
A.C(s)+H2O(g) CO(g)+H2(g) ΔH>0
CO(g)+H2(g) ΔH>0
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l) ΔH<0
NaCl(aq)+H2O(l) ΔH<0
C.2H2(g) +O2(g) 2H2O(l) ΔH<0
2H2O(l) ΔH<0
D.CaCO3(s)+2HCl(aq) CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
CaCl2(aq)+H2O(l)+CO2(g) ΔH<0
E.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH<0
CO2(g)+2H2O(l) ΔH<0
(2)有A、B、C、D四种金属,将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等物质的量浓度的盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化,如果把铜浸入C的盐溶液里,有金属C析出。据此判断A、B、C、D的活动性由强到弱的顺序是 。
Ⅰ.现有八种微粒:Na、Mg2+、Fe2+、Fe3+、S2-、SO2、HCl、H2O,从元素化合价的角度分析,其中只有氧化性的是______,只有还原性的是______,
既有氧化性又有还原性的是___________。
Ⅱ.已知能用氯酸钾与浓盐酸反应制取氯气,其化学方程式如下:
KClO3+6HCl=KCl+3Cl2↑+ 3H2O
⑴用单线桥在上述方程式中标出电子转移的方向和数目。
⑵标况下生成3.36LCl2,转移电子的物质的量为,被氧化的盐酸与未被氧化的盐酸质量之比为。氧化产物与还原产物物质的量之比为。
Ⅰ.某化学兴趣小组对下列三组物质进行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液水悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
| A |
B |
C |
|
| 分类标准 |
含氧酸 |
分散系 |
|
| 不属于该类别的物质 |
Na2CO3 |
Ⅱ.现有下列物质:①铝②氢氧化铁胶体③氯化氢④SO2 ⑤NaHSO4固体⑥Ba(OH)2固体 ⑦稀硫酸⑧醋酸⑨烧碱⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
| 分类标准 |
能导电的物质[ |
电解质 |
强电解质 |
| 属于该类的物质 |
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。
(1)18gH2O的物质的量是,含有个氢原子(填具体数字);这些H2O与 gOH-所含电子数相等。
(2)标准状况下,①6.72L CH4②3.01×1023HCl分子 ③0.2molNH3 ,这三种气体按物质的量由大到小排列的顺序是(填物质的数字代号,下同),按氢原子数由多到少排列的顺序是,密度由大到小排列的顺序是。
A、B、C、D、E为前四周期元素,原子序数依次增大。基态A原子的核外电子占据4个原子轨道;B与C同主族,大气平流层中单质B3浓度减少会致人患皮肤癌增加;D是前四周期元素中第一电离能最小的元素;E的合金是当今用量最大的合金。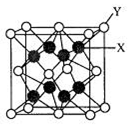
(1)E在同期表中的位置是,其基态原子的简化电子排布式为。
(2)CB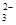 的立体构型是。
的立体构型是。
(3)D2C的晶胞结构与CaF2晶胞(如图)相似,则Y应为(填离子符号);D2C的熔点比CaF2熔点(填“高”、“低”或“无法比较”)。
A、B、C、D代表4种元素,请完成下列问题
(1)A元素的基态原子的最外层有3个未成对电子,次外层有2个电子,A元素的名称是,该元素的原子核外共有 种不同运动状态的电子;该元素的第一电离能比后面一号元素大的原因是。
(2)B为元素周期表中的29号元素,常与H2O、NH3等形成配合物。
B的无水硫酸盐晶体呈色,向盛有B的硫酸盐水溶液的试管里逐滴加入氨水,首先形成,继续添加氨水,沉淀溶解得到,写出后一步反应的离子方程式。
(3)C元素的负一价离子的电子层结构与氩相同,C的最高价氧化物的水化物的化学式为。
(4)A元素的最高价氧化物对应的水化物的稀溶液与29号元素的单质反应的离子方程式是____________________。
(5)D元素在元素周期表的各元素中,电负性仅小于氟,A的最低价氢化物与D的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为___________________。