某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
| A.1∶2 | B.1∶4 | C.3∶4 | D.3∶2 |
关于下列图示的说法中不正确的是()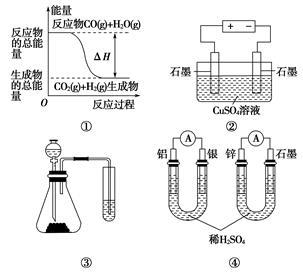
| A.图①表示CO(g)+H2O(g)===CO2(g)+H2(g)是放热反应 |
| B.图②为电解硫酸铜溶液的装置,电解一段时间后,加入一定量的Cu(OH)2一定不能使溶液恢复到电解前的浓度和体积 |
| C.图③实验装置可一次而又科学准确地完成比较HCl、H2CO3、H2SiO3酸性强弱的实验 |
| D.图④两个装置中通过导线的电子数相同时,正极生成气体的物质的量也相同 |
(双选)下列说法不正确的是()
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的ΔH>0 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D.相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是()
| A.若pH>7,则一定是c1V1=c2V2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c2>c1 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
按甲图所示装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是()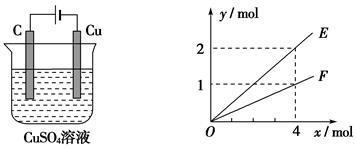
甲乙
| A.E表示生成铜的物质的量 |
| B.E表示总反应中消耗水的物质的量 |
| C.F表示反应生成氧气的物质的量 |
| D.F表示生成硫酸的物质的量 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)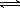 2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是()
2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是()
| A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |