制造硫酸的工艺流程反应其中之一是2SO2(g)+O2(g)←→2SO3(g)+190 kJ。下列描述中能说明上述反应已达平衡的是
| A.v(O2)正=2v(SO3) |
| B.容器中气体的平均摩尔质量不随时间而变化 |
| C.如果容器容积是固定的,那么混合气体的密度不随时间而变化 |
| D.单位时间内生成n mol SO3的同时生成n mol O2 |
把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s)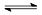 Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是()
Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是()
| A.溶液中Ca2+数目减少 | B.溶液中c(Ca2+)增大 |
| C.溶液中c(Ca2+)减小 | D.溶液pH值增大 |
一定条件下,在体积为10L的密闭容器中,1 molX和1 molY进行反应:2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是 ( )
Z(g),经60s达到平衡,生成0.3molZ,下列说法正确的是 ( )
| A.以X浓度变化表示的反应速率为0.001mol/(L·s) |
| B.将容器体积变为20L,Z的平衡浓度变为原来的1/2 |
| C.若升高温度Y的转化率减小,则正反应为吸热反应 |
| D.达到平衡时,X与Y的浓度相等 |
下列各溶液中,微粒的物质的量浓度关系正确的是()
| A.0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B.0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)>c(NO3-) |
下列叙述正确的是()
| A.可以根据PbI2和AgCl的Ksp的大小比较两者的溶解能力 |
| B.常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大 |
| C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
| D.能使碘化钾淀粉试纸变蓝的溶液中,Na+、S2-、Br-、NH4+等离子可以大量共存 |
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应为:C2H6 + 18OH-→2CO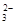 + 12H2O + 14e-;14H2O + 7O2 + 28e-→28OH-,有关推断错误的是()
+ 12H2O + 14e-;14H2O + 7O2 + 28e-→28OH-,有关推断错误的是()
| A.通氧气的电极为正极 |
B.在电解质溶液中CO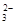 向正极移动 向正极移动 |
| C.放电一段时间后,KOH的物质的量浓度将下降 |
| D.参加反应的氧气和乙烷的物质的量之比为7:2 |