常温下,下列各组离子在指定的条件下一定能大量共存的是
| A.水电离的氢离子浓度为10-6 mol/L的溶液中:Na+、HCO3- 、Br -、Cl- |
| B.pH=7的溶液中:Fe3+、Cu2+、Cl-、SO42- |
| C.使酚酞变红的溶液中:Ba2+、Cl-、Na+、NO3- |
| D.加入铝粉产生氢气的溶液:Na+、Cu2+、Cl-、NO3- |
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
| A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
某有机化合物的结构简式为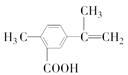 ,有关该化合物的叙述不正确的是
,有关该化合物的叙述不正确的是
| A.该有机物的分子式为C11H12O2 |
| B.1 mol该物质最多能与4 mol H2发生加成反应 |
| C.该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀 |
| D.该有机物一定条件下,可以发生取代、氧化、酯化反应 |
已知AgCl的溶解度为1.5×10-4g , AgBr的溶解度为8.4×10-6g ,如果将AgCl和 AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生反应的结果为
| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀多于AgBr沉淀 | D.AgCl沉淀少于AgBr沉淀 |
现有某氯化物与氯化镁的混合物,取3.8g粉末完全溶于水后,与足量的硝酸银溶液反应后得到12.4 g氯化银沉淀,则该混合物中的另一氯化物是
| A.FeCl3 | B.KCl | C.CaCl2 | D.LiCl |
用下列装置进行相应实验,能达到实验目的的是
| 选项 |
A |
B |
C |
D |
| 装置 |
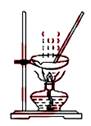 |
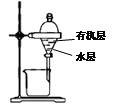 |
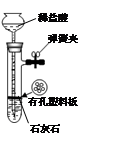 |
 |
| 目的 |
蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
分离CCl4萃取碘水后已分层的有机层和水层 |
制取少量CO2气体 |
除去Cl2中含有的少量HCl |