Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:
2FeSO4 + a Na2O2 = 2Na2FeO4 + b X + 2Na2SO4 + c O2↑
该反应中物质X应是 ________ ,b与c的关系是 ___________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式: _________________。
②每生成1mol FeO42-转移 _______ mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 mo1。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是____________,被氧化的离子的物质的量分别是_______________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为_______________(用含a、b的代数式表示)。
(1)现有浓度各为1 mol/L的FeCl3、FeCl2、CuCl2的混合溶液100mL,加入一定量的铁粉,按下列情况填空:
①充分反应后铁粉有剩余,则溶液中一定含有__________阳离子,一定没有__________阳离子。有关反应的离子方程式是__________________________
__________________________________________________________。
②充分反应后铁粉无剩余,有铜生成。则反应后的溶液中一定含有_________阳离子;溶液中可能含有_________阳离子,该阳离子在溶液中物质的量的可能存在范围是: ______________________。
③充分反应后,无固体沉淀物存在,反应后的溶液中一定含有____和____阳离子。
(2)现有AlCl3和FeCl3的混合溶液,其中Al3+和Fe3+的物质的量之和为0.1 mol。在此溶液中加入90 mL 4 mol / L的NaOH溶液,使其充分反应;设Al3+ 的物质的量与总物质的量的比值为x。
①根据反应的化学方程式计算x=0.4时,溶液中产生的沉淀是___________;物质的量是__________mol。
②计算沉淀中只有Fe(OH)3时的x的取值范围:_____________________。
下列图中A-F是中学化学常见化合物,且A﹑B﹑E﹑F均含有相同一种金属元素,G是一种常见单质。
①A(固体) B + C + D②C + E → B + G;③ D + E → F + G
B + C + D②C + E → B + G;③ D + E → F + G
④A(溶液)+F(溶液)→B(溶液)+D⑤B(溶液) + C + D → A(溶液)
(1)写出A﹑B﹑C﹑E﹑F的化学式:A__________ B_________ C__________
E__________ F__________
(2)写出反应①②④⑤的化学方程式:
①_________________________________________________
②_________________________________________________
④_________________________________________________
⑤_________________________________________________
(3)请写出化合物E的两种重要用途:____________________________
(6分)有一瓶澄清的溶液,其中可能含NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-、I-,取该溶液进行如下实验:
⑴用pH试纸检验,表明溶液呈强酸性;
⑵取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置CCl4层呈紫红色;
⑶取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
⑷取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑸将⑶得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:
在溶液中肯定存在的上述离子有 ,肯定不存在的上述离子有 。
(6分)下列事实反映了硝酸的什么性质:①不稳定性②强氧化性③强酸性
⑴硝酸应贮存在棕色试剂瓶中 ;⑵Ag与稀硝酸作用制取AgNO3 ;⑶可用稀硝酸与CaCO3作用制取CO2。
(7分)如图所示:在上述转化关系中,已知B、D都是淡黄色固体,且A与D可反应生成离子化合物A2D。回答: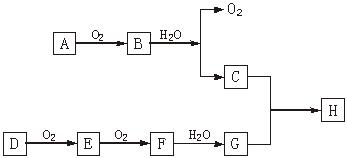
(1)写出下列物质的化学式A._______,H._______。
(2)写出C的电子式_______,B中含有的化学键类型是
(3)写出E→F的化学方程式。