检验某溶液中是否含有K+、Fe3+、Cl﹣、Mg2+、I﹣、CO32﹣、SO42﹣,限用的试剂有:盐酸硫酸、硝酸银溶液、硝酸钡溶液.设计如下实验步骤,并记录相关现象.下列叙述不正确的是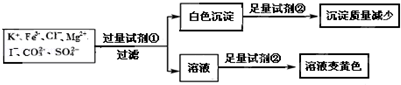
| A.该溶液中一定有I﹣、CO32﹣、SO42﹣、K+ |
| B.试剂①为硝酸钡 |
| C.通过黄色溶液中加入硝酸银可以检验原溶液中是否存在Cl﹣ |
| D.试剂②一定为盐酸 |
标准状况下H2和Cl2组成的混合气体2.24L,经点燃充分反应后,缓缓通入100mL1.2mol/LNaOH溶液中恰好完全反应,测得最终溶液中NaClO的浓度为0.2mol/L(假设溶液体积不变),则原混合气体中Cl2的体积分数(物质的量百分含量)为
| A.55% | B.60% | C.65% | D.70% |
下列离子方程式正确的是
| A.Zn和浓硫酸反应:Zn+2H+=H2↑+Zn2+ |
| B.钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| C.硫酸铝溶液与过量氢氧化钠溶液反应:Al3+ +4OH—=AlO2-+2H2O |
| D.向Ca(ClO)2溶液中通入少量CO2:ClO-+H2O+CO2=HClO+HCO3- |
下列实验过程中,始终无明显现象的是
| A.向Al2(SO4)3溶液中通入NH3 | B.向NaHCO3溶液中滴入烧碱溶液 |
| C.向淀粉-KI溶液中通入NO2气体 | D.向含酚酞的NaOH溶液中通入SO2气体 |
下列关于物质性质的说法正确的是
| A.二氧化硅既溶于强酸,又溶于强碱 |
| B.铁在纯氧中的燃烧产物是红棕色固体 |
| C.盐酸滴加到水玻璃中,可以产生白色胶状物质 |
| D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
| A.8 g甲烷含有的共价键数约为NA |
| B.常温常压下,22.4 L二氧化碳原子总数为3NA |
| C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子 |
| D.3.2g硫(结构见图)含S-S键的数目为0.8NA |
