下列反应中,属于加成反应的是
| A.CH3Cl+Cl2 → CH2Cl2 + HCl |
| B.CH2=CH2+HO﹣H → HOCH2﹣CH3 |
C.2CH3CH2OH+O2 2CH3CHO + 2H2O 2CH3CHO + 2H2O |
D. +Br2 +Br2  + HBr + HBr |
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+==Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol。下列说法正确的是()
| A.反应中硫元素被氧化,所有铁元素均被还原 |
| B.氧化剂是Fe3+,氧化产物是Cu2+ |
| C.反应中转移电子的物质的量为x mol |
| D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol |
将35.8g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
| A.66.4 g | B.50.8 g | C.44.8g | D.39.2g |
下列有关操作或判断正确的是()
| A.配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高 |
| B.用托盘天平称取25.20 g NaCl |
| C.用100 mL的量筒量取5.2 mL的盐酸 |
| D.用浓盐酸配制一定物质的量浓度的稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高 |
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1,质量分数为w,其中含有NH4+的物质的量是b mol,下列叙述正确的是()
A.溶质的质量分数w=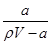 ×100% ×100% |
B.溶质的物质的量浓度c=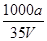 mol·L-1 mol·L-1 |
C.溶液中c(OH-)=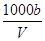 mol·L-1+c(H+) mol·L-1+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w |
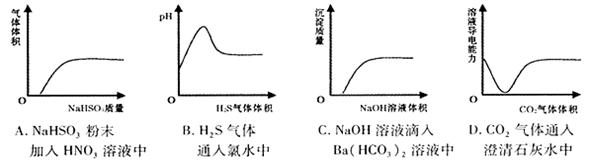
下列实验过程中的有关变化与对应的图形相符合的是()