节能减排对发展经济、保护环境有重要意义。下列措施不能减少二氧化碳排放的是
| A.利用太阳能制氢 |
| B.关停小火电企业 |
| C.举行“地球一小时”熄灯活动 |
| D.推广使用煤液化技术 |
体积为V mL,密度为d g/mL,溶质的摩尔质量为M g·mol-1,物质的量浓度为c mol·L-1,溶质的质量分数为a%,溶质的质量为m g。下列式子正确的是
| A.m=aV/100d | B.c=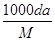 |
C.c= |
D.a%=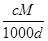 % % |
下列条件下,两物质所含分子数不相等的是
| A.同温度、相同质量的N2和CO | B.常温常压,同体积的H2O和O2 |
| C.同压强、同物质的量的N2和O2 | D.同体积、同密度的N2和CO |
在无色透明酸性溶液中,能大量共存的离子组是
| A.Mg2+、NO3-、Cl、Na+ | B.K+、SO42-、HCO3-、Na+ |
| C.NH4+、NO3-、Al3+、CH3COO | D.MnO4-、K+、SO42-、Na+ |
下列各组物质中所含分子数一定相同的是
| A.5.6L N2和11g CO2 | B.5g CO和5g H2 |
| C.含1mol H原子的H2O和0.5mol Br2 | D.质子数相等的NH3和HCl |
纳米碳是一种重要的“纳米材料”,其粒子直径为1~100 nm之间。若将纳米碳均匀地分散到蒸馏水中,所形成的分散系是:①溶液 ②胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤能透过半透膜 ⑥静置会析出黑色沉淀。其中正确的是
| A.②⑤⑥ | B.②③⑤⑥ | C.②③④ | D.①③④ |