肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气。已知:N2(g)+2O2(g)===N2O4(g) ΔH=+8.7 kJ/mol,N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534.0 kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是
| A.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g)ΔH=-542.7 kJ/mol |
| B.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 059.3 kJ/mol |
| C.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g)ΔH=-1 076.7 kJ/mol |
D.N2H4(g)+ N2O4(g)=== N2O4(g)===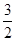 N2(g)+2H2O(g)ΔH=-1 076.7 kJ/mol N2(g)+2H2O(g)ΔH=-1 076.7 kJ/mol |
下列除去杂质的方法正确的是()
| A.除去CO2中混有的CO:用澄清石灰水洗气 |
| B.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| C.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
wg铁粉和铝粉的混合物,和过量的 NaOH反应,然后过滤,将沉淀完全收集后,放蒸发皿中加热,直至被加热的物质质量不再变化,取出蒸发皿中的物质称量仍为wg。求原混合物中铝粉的质量分数是()
| A.30% | B.50% | C.70% | D.90% |
设NA表示阿伏加德罗常数的值。下列说法正确的是()
| A.标准状况下,0.1 mol Cl2溶于足量水,转移的电子数目为0.1NA |
| B.0.1 mol Fe 与足量的稀HNO3反应,转移0.2N A个电子 |
| C.1 L 0.1 mol·L-1 Na2CO3溶液含有0.1NA 个CO3 2- |
| D.电解熔融NaCl得到7.1g Cl2,理论上需要转移0.2NA个电子 |
化学知识在生产和生活中有着重要的应用。下列说法中正确的是()
①钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等
②K、Na合金可作原子反应堆的导热剂
③发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔④Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂
| A.①②③④ | B.①②③④⑤ | C.①②③④⑥ | D.①②③④⑤⑥ |
常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A.MnO2 CuO FeO | B.(NH4)2SO4K2SO4NH4Cl |
| C.AgNO3 KNO3 Na2CO3 | D.Na2CO3 NaHCO3 K2CO3 |