某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol·L-1 HNO3、2.00 mol·L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
(1)他们能完成哪些因素对速率影响的探究?____________________。
(2)请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
| 实验编号 |
T/℃ |
大理石规格 |
HNO3浓度/mol·L-1 |
| ① |
常温 |
细颗粒 |
2.00 |
| ② |
|
细颗粒 |
1.00 |
| ③ |
35℃ |
|
2.00 |
| ④ |
35℃ |
|
2.00 |
(3)整个实验中应控制的不变量是硝酸溶液体积和 。
(4)该实验小组用如图实验装置进行实验。
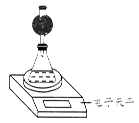
①除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有___ _____。
②干燥管中应放置的试剂是________。
A.碱石灰 B.无水CaCl2
C.P2O5固体 D.浓硫酸
③若撤除干燥管装置,所测速率________(填“偏大”、“偏小”或“不变”)。
掌握物质之间的转化,是学习元素化合物知识的基础。
(1)中学常见的某反应的化学方程式为:A+B→C+D+H2O(未配平,反应条件略去)。
若C、D均为气体,且都能使澄清石灰水变浑浊。
①请写出该反应的化学方程式 ;
②某探究性学习小组利用图中所列装置实验,证明上述反应中有C、D生成。则a瓶对应的现象是 ,b瓶溶液还可以用 代替。
③装置d中所盛溶液是 。
(2)为研究硝酸置于适量的浓HNO3和稀HNO3中(如下图所示)。
①气球的作用是 。
②A中,最终溶液变为浅绿色,发生反应的离子方程式是 。
③B中,无明显变化,该同学进一步探究如下:
假设:Ⅰ常温下铁与浓硝酸不反应。
Ⅱ 。
进行实验,将B中的铁片取出并洗净后,放入CuSO4溶液中,无明显变化,则说明假设Ⅰ (填“成立”或“不成立”)。
长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
【查阅资料】CaO2与Na2O2具有相似的化学性质。
【提出问题】当CaO2投入足量水中时,最终会生成什么物质呢?
【进行猜想】甲同学认为,生成氧化钙和氧气;乙同学认为,生成氢氧化钙和氧气。
(1)甲同学的猜想明显是错误的,其理由是________________________。
(2)写出乙同学猜想发生反应的化学方程式________________________。
【实验验证】
(3)一同学设计如下实验:取少量CaO2放入试管中,加足量水充分反应,待没有气体逸出时,滴加几滴_____________,观察到溶液变红,则证明有氢氧化钙生成。乙同学发现红色很快褪去了。他通过查阅资料了解到还生成了一种曾经学习过的物质,请你猜测该物质是_____________。
(4)请你利用如图所示装置设计实验予以证明。
X中CaO2与水充分反应后的溶液,Y中的固体物质为__________________。打开分液漏斗活塞,使X中溶液滴下,_________(补充完后续试验的操作、现象),则证明你的猜测合理。
某学习小组研究“不同条件对化学反应速率影响的探究”,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液在稀硫酸中进行实验,改变条件如表:
| 组别 |
草酸的体积 /mL |
温度/℃ |
其它物质 |
| ① |
2 mL |
20 |
|
| ② |
2 mL |
20 |
2滴饱和MnSO4溶液 |
| ③ |
2 mL |
30 |
|
| ④ |
1 mL |
20 |
1 mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用 ①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
工业上将纯净干燥的氯气通入到0.5 mol·L-1 NaOH溶液中得到漂白水。
某同学想在实验室探究Cl2性质并模拟制备漂白水,上图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(注:装置D中布条为红色)
(1)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O
(2)如果反应中转移0.5mol电子,则生成Cl2的物质的量为_______________。
(3)浓硫酸的作用是 。
(4)实验时装置D中的现象是 。
(5)装置E中发生化学反应的离子方程式为 。
(6)配制500 mL物质的量浓度为0.5 mol·L-1 NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需称量的NaOH的质量是 。
在如下图装置中,用NaOH溶液、铁屑、稀硫酸等试剂制备Fe(OH)2。
(1)在试管I中加入的试剂是 。
(2)为了制得Fe(OH)2白色沉淀,在试管I和Ⅱ中加入试剂,打开止水夹,塞紧塞子后观察到试管I产生大量气体。一段时间后,检验到试管Ⅱ支管出口的气体只有一种时,再进行的操作是 ,使试管I中的溶液进入到试管Ⅱ中溶液底部,产生Fe(OH)2。
(3)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是 。
(4)反应结束后,将Fe(OH)2沉淀倒出,在空气中迅速变为灰绿色,最后变为红褐色,其原因是 (用化学方程式表示)。