现有4.6gNa、2.4gMg、2.7gAl和6.4gCu,分别将其投入盛有100mL1.5mol/L盐酸的4个烧杯。
(1)各烧杯中可能发生反应的化学方程式为:___________、_____________、__________、______________。
(2)反应结束后,没有剩余的金属是:__________(填元素符号);
(3)反应结束后,产生气体的物质的量分别为:
①投入Na的烧杯,生成气体____mol;
②投入Mg的烧杯,生成气体____mol;
③投入Al的烧杯,生成气体____mol;
④投入Cu的烧杯,生成气体____mol;
取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式:,反应后得到的溶液呈色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为,此反应属于。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到烧杯中的液体产生丁达尔效应。这个实验可以用来区别。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
①先出现红褐色沉淀,随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:。
②最后溶液颜色加深,原因是。(用离子方程式表示)。
③用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象(写序号)。
在如下图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种黑色粉末,D为一种气体。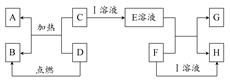
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为;D可能为。
(2)若G为蓝色沉淀,H为难溶性盐,则I为。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为;F可能为。
以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空: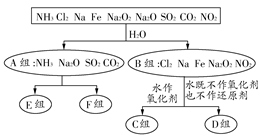
(1)上述第一级分类标准(分成A、B组所依据)是。
(2)C组物质为。
(3)D组物质中,与水反应时氧化剂和还原剂的物质的量之比为1:1的物质是(填化学式)。
(4)若E组和F组均有两种物质,则其分类依据是。
在建国60周年阅兵仪式上,我国展示的歼10、歼11等新型飞机,大展国威,为我们的平安生活筑起了新的“万里长城”,新型武器中离不开新材料的使用。请完成下列问题:
(1)下列说法不正确的是。
A.飞机机身材料(镁铝合金)经过抗氧化处理,能有效防止腐蚀
B.飞机中的导线外层可能由PVC材料制成
C.碳纤维材料可用于制造大型飞机通讯设备的外壳
D.飞机使用的机舱玻璃可由玻璃钢制成
(2)飞机上使用的某复合材料的基体是氮化硅陶瓷,增强体是SiO2纤维。
对该复合材料的说法正确的是。
A.该复合材料性质很稳定,不会溶解在任何酸中
B.氮化硅的化学式为Si3N4
C.该复合材料耐高温,强度高,导电导热性好,不易老化,可用于制造精密电子仪器
D.该复合材料与玻璃钢性能相似
(3)无氧铜是用于制造飞机所需真空电子器件的重要材料,但是无氧铜含氧超标会造成真空电子构件不合格,这仍是国际上的技术难题。一般所说的铜中含氧,实际上指的是含有Cu2O。某化学兴趣小组对一份铜样品展开探究(已知:Cu2O与Cu均为红色固体,酸性条件下能发生反应:Cu2O+2H+=Cu+Cu2++H2O)。
甲同学取少量该红色试样溶于过量的稀硝酸;乙同学取少量该红色试样溶于过量的稀硫酸。甲、乙的实验中能判断样品中是否含有Cu2O的是。甲同学的实验现象是。
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、
负极,并写出电极反应式。
正极反应:。
负极反应:。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤。
| 氢氧化物开始沉淀时的pH |
氢氧化物沉淀 完全时的pH |
|
| Fe3+ Fe2+ |
1.9 7.0 |
3.2 9.0 |
| Cu2+ |
4.7 |
6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。有关反应的化学方程式;;劣质不锈钢腐蚀的实验现象。