普通锌锰干电池的外壳是锌筒,内置一个碳棒作电极,工作时发生的反应为:
下列有关说法不正确的是
| A.干电池的负极是锌筒 | B.MnO2在碳棒上发生还原反应 |
| C.闲置时间过长干电池也会失去供电能力 | D.工作时电解液中的NH4+移向负极 |
下列物质中,属于纯净物的是
| A.液氯 | B.氯水 | C.稀盐酸 | D.漂白粉 |
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是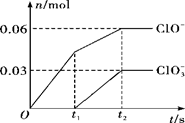
| A.Cl2和苛性钾溶液在不同温度下可能发生不同反应 |
| B.反应中转移电子数为是0.21 NA |
| C.原苛性钾溶液中KOH的物质的量无法确定 |
| D.生成物中Cl- 的物质的量为 0.21 mol |
把NaHCO3和Na2CO3.10H2O混合6.56克溶于水,制成100ml溶液,其中Na+物质的量浓度为0.5mol/L ,若将等质量的该混合物加热至恒重,所得固体质量为
| A.2.65 g | B.3.91 g | C.5.3 g | D.4.23g |
将足量CO2通入NaOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(v)的关系正确的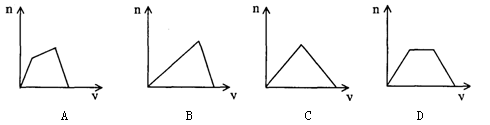
类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是
| 已知 |
类推 |
|
| A |
将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ |
将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
| B |
向稀硫酸加入NaOH溶液至中性 H++OH-=H2O |
向H2SO4溶液加入Ba(OH)2溶液至中性 H++OH-=H2O |
| C |
向氯化铝溶液中加入足量NaOH溶液 Al3+ + 4OH- = AlO2- + 2H2O |
向氯化铝溶液中加入足量氨水 Al3+ + 4NH3·H2O = AlO2- + 2H2O +4NH4+ |
| D |
向Ca(OH)2溶液中通入过量CO2 CO2 + OH- = HCO3- |
向Ca(OH)2溶液中通入过量SO2 SO2 + OH- = HSO3- |