下列有关叙述中正确的是
| A.CH4与P4的分子结构都是正四面体形,因此在6.02×1023个CH4分子或P4分子中都含有4×6.02×1023个共价键 |
| B.在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键 |
| C.5.6 g Fe与含0.2 mol HNO3的溶液充分反应,至少失去0.2×6.02×1023个电子 |
| D.6.02×1023个Fe3+完全水解可以得到6.02×1023个氢氧化铁胶体粒子 |
将下列溶液蒸干、并灼热后,仍能得到原溶质固体的是
| A.AlCl3溶液 | B.NaAlO2溶液 | C.NaHCO3溶液 | D.FeSO4溶液 |
反应FeO(s)+C(s)=Fe(s)+CO(g); △H>0,ΔS>0,下列说法正确的是
| A.低温下自发进行,高温下非自发进行 | B.高温下自发进行,低温下非自发进行 |
| C.任何温度下均为非自发进行 | D.任何温度下均为自发进行 |
常温下,某溶液中由水电离出的出c(H+)=1.0 ×10—13mol/L则在该溶液中一定不可以大量共存的一组离子是
| A.NH4+、NO3—、K+、SO42— | B.CO32_、NO3—、HCO3—、Na+ |
| C.Na+、ClO—、AlO2—、NO3— | D.MnO4—、K+、Na+、SO42— |
下列各反应的化学反应方程式或离子反应方程式中,属于水解反应的是
A.CO32-+H2O HCO3-+OH- HCO3-+OH- |
B.HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
C.CO2+H2O H2CO3 H2CO3 |
D.H2O+H2O H3O++OH- H3O++OH- |
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:
Ca(OH)2(s) 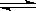 Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
| A.c(Ca2+)增大 | B.c(Ca2+)不变 |
| C.c(OH-)增大 | D.Ca(OH)2固体的质量不变 |