2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。青蒿素分子式C15H22O5,相对分子质量为282.下面关于青蒿素的说法正确的是
| A.1 mol C15H22O5的质量为282 g/mol |
| B.C15H22O5的摩尔质量等于它的相对分子质量 |
| C.一个C15H22O5微粒的质量约为 282/(6.02×1023)g |
| D.含有6.02×1023个碳原子的C15H22O5的物质的量为1 mol |
化学中常用图象直观地描述化学反应的进程或结果。下列图象描述正确的是
通过复习总结,下列归纳正确的是
| A.Na2O,NaOH,Na2CO3,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物 |
| B.简单非金属阴离子只有还原性,而金属阳离子不一定只有氧化性 |
| C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| D.物质发生化学变化一定有化学键断裂与生成,并伴有能量变化,而发生物理变化就一定没有化学键断裂与生成,也没有能量变化 |
下列反应的离子方程式不正确的是
| A.向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| C.足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓ |
| D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
下列示意图与对应的反应情况正确的是
| A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.NaAlO2溶液中逐滴加入盐酸 |
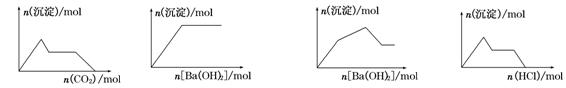
A BCD
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是
| A.铝钠合金是混合物 |
| B.铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |