下列与金属腐蚀有关的说法正确的是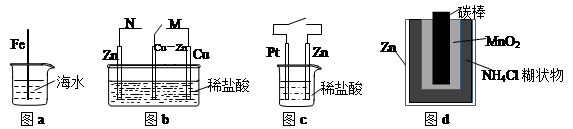
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu—Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn—MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如下图所示,下列判断正确的是
| A.a、c两点溶液的导电能力相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.a、b、c三点溶液水的电离程度a>b>c |
| D.与等体积b、c处溶液反应,消耗等量的NaOH |
有关下图电化学装置的叙述中,正确的是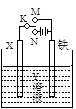
| A.若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气 |
| B.若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加 |
| C.若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护 |
| D.若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe−2e→Fe2+ |
已知:S(s)+O2(g)→SO2(g) +297.16kJ,2SO2(g)+O2(g) 2SO3(g)+196.6 kJ,下列说法正确的是
2SO3(g)+196.6 kJ,下列说法正确的是
| A.1 molSO2(g)的能量总和大于lmol S(s)和l molO2(g)的能量总和 |
| B.将2 molSO2(g)与l molO2(g)在一定条件下充分反应,放出196.6kJ的热量 |
C.S(g)+O2(g) SO2(g)+Q,Q值小于297.16 kJ SO2(g)+Q,Q值小于297.16 kJ |
| D.当l mol S(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
下列事实不能用勒夏特列原理解释的是
| A.配制氯化铁溶液时,加入少量稀盐酸 |
| B.配制氯化亚铁溶液时,加入少量铁屑 |
| C.在含有酚酞的氨水中加入少量NH4Cl,溶液颜色会变浅 |
| D.在硫酸铜饱和溶液中加入一块胆矾,晶体外形变规则 |
原子晶体干冰具有类似SiO2的晶体结构,下列有关它的推断中,错误的是
| A.它可作耐磨材料 |
| B.它不可用作致冷剂 |
| C.晶体中每个碳原子形成2个碳氧双键 |
| D.晶体中碳、氧原子个数之比为1:2 |