甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,将丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是
| A.Al2(SO4)3 | B.NaOH | C.BaCl2 | D.FeSO4 |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为
a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。下列有关说法不正确的是
| A.由反应可确定:氧化性HClO3>O2 |
| B.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O |
| C.由非金属性Cl>S,可推知酸性HClO3>H2SO4 |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
下列现象或事实不能用同一原理解释的是
| A.浓硝酸和氯水用棕色试剂瓶保存 |
| B.硫化钠和亚硫酸钠固体长期暴露在空气中变质 |
| C.常温下铁和铂都不溶于浓硝酸 |
| D.SO2和Na2SO3溶液都能使氯水褪色 |
下列各种溶液中通入足量的SO2后,既无沉淀又无气体产生的是
①NaClO ②C6H5ONa ③Na2S④BaCl2⑤Ba(OH)2⑥H2O2
| A.①④⑥ | B.①②③ | C.④⑤⑥ | D.①④⑤⑥ |
下列装置所示的实验不能达到目的的是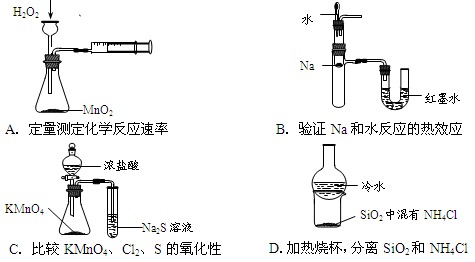
将下图中所示实验装置的K闭合,下列判断正确的是 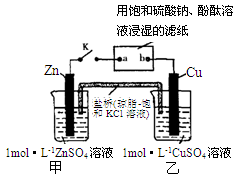
| A.电子沿Zn→a→b→Cu路径流动 |
| B.Cu电极上发生氧化反应 |
| C.甲池与乙池中的溶液互换,闭合K仍有电流产生 |
| D.片刻后可观察到滤纸a点变红色 |