在一定温度下,在体积可变的容器中,进行可逆反应A(g) + B(g) C(g) + 2D(g);下列能说明该反应达到平衡状态的是
C(g) + 2D(g);下列能说明该反应达到平衡状态的是
①反应混合物的密度不再改变 ②混合气体的平均相对分子质量不再改变 ③C和D的物质的量之比为1:2 ④体系压强不再改变 ⑤C的质量分数不再改变 ⑥υ(A) : υ(C) =" 1:" 1
A.①②④⑤ B.①②⑤ C.②⑤⑥ D.①②③④⑤⑥
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标志中的( )
A.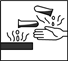 |
B. |
C. |
D. |
下列叙述正确的是
| A.含1.00mol NaCl的水溶液中,含有的分子数应多于6.02×1023 |
| B.在标准下,11.2L水所含有的电子总数为5×6.02×1023 |
| C.欲配置1.00L 、1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.将氯化钡溶液加入蛋白质溶液中使其发生盐析而达到分离蛋白质的目的。 |
下列各组物质的稀溶液相互反应,无论是前者滴入后者还是后者滴入前者,反应现象相同的是
| A.AlCl3和NaOH | B.硫酸铝和浓氨水 |
| C.NaAlO2和H2SO4 | D.氨水和AgNO3溶液 |
向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
| A.0.24mol | B.0.21mol | C.0.16mol | D.0.14mol |
下列说法正确的是
| A.产物中的氧化物不可能是还原产物,只可能是氧化产物 |
| B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| C.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |