五氯化磷(PCl5)是有机合成中重要的氯化剂,可以有三氯化磷(PCl3)氯化得到: 。某温度下,在容积恒定为2.0L的密闭容器中充入2.0molPCl3和1.0molCl2,一段时间后反应达平衡状态,实验数据如下表所示:
。某温度下,在容积恒定为2.0L的密闭容器中充入2.0molPCl3和1.0molCl2,一段时间后反应达平衡状态,实验数据如下表所示:
(1) 0~150s内的平均反应速率
(2) 该温度下,此反应的化学平衡常数的数值为___________(可用分数表示)。
(3) 反应至250s 时,该反应放出的热量为______________kJ。
(4) 下列关于上述反应的说法中,正确的是__________(填字母序号)。
a. 无论是否达平衡状态,混合气体的密度始终不变
b. 300s 时,升高温度,正、逆反应速率同时增大
c. 350s 时,向该密闭容器中充入氮气,平衡向正反应方向移动
d. 相同条件下,若起始向该密闭容器中充入1.0molPCl3和0.2molCl2,达到化学平衡状态时,n(PCl5 ) < 0.20mol
(5) 温度T 1时,混合气体中PCl5 的体积分数随时间t 变化的示意图如下。其他条件相同,请在下图中画出温度为T 2(T 2> T 1)时,PCl5的体积分数随时间变化的曲线。
橙皮素具有抗氧化、消炎、降血脂、保护心血管和抗肿瘤等多种功效。它的合成路线如下: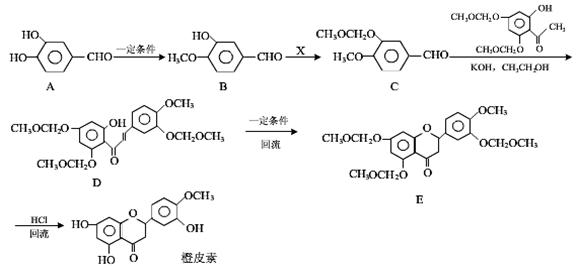
⑴化合物A中的含氧官能团除酚羟基外还有(填官能团名称)。
⑵已知:B→C为取代反应,其另一产物为HCl,写出X 的结构简式:。
⑶反应D→E的反应类型是。
⑷写出同时满足下列条件的B的同分异构体的结构简式:。
Ⅰ.属于芳香族化合物;
Ⅱ.分子中有4种不同化学环境的氢;
Ⅲ.不能与FeCl3溶液发生显色反应,但能发生水解反应。
⑸如何由CH3CH2CH2Br制备CH3CH(OH)CH2OH,请设计流程图并写出每一步的化学方程式
(合成路线流程图示例如下: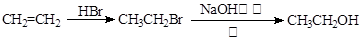 )
)
某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀CuI。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
已知:I2+2S2O32-=S4O +2I-
+2I-
①可选用_____作滴定指示剂,滴定终点的现象是_______________________________ 。
②CuCl2溶液与KI反应的离子方程式为_______________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
(1)MgCO3与稀硫酸反应的离子方程式为。
(2)加入H2O2氧化时,发生反应的化学方程式为。
(3)滤渣2的成分是(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C  2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C  MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C  MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集
①D中收集的气体是。
②B中盛放的溶液可以是。
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
电镀厂镀铜废水中含有CN-和Cr2O72-离子,需要处理达标后才能排放。该厂拟定下列流程进行废水处理,回答下列问题:
(1)②中反应后无气体放出,该反应的离子方程式为______________;
(2)步骤③中,每处理0.4mol Cr2O72-时转移电子2.4mol,该反应的离子方程式为;
(3)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,请用离子方程式解释产生这些现象的原因;
(4)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4 ·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于: (铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4 • 7H2O,下列结论正确的是_______。
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1mol Cr2O72-,需加入a mol FeSO4 • 7H2O,下列结论正确的是_______。
| A.x =0.5,a =8 | B.x ="0.5" ,a =" 10" |
| C.x = 1.5,a =8 | D.x =" 1.5" ,a = 10 |
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e-→NO↑+2H2O
KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的离子方程式:
(2)若有0.3mol甲参加反应,标准状况下可生成NOL。