赤铁矿是常用的炼铁原料,其主要成分为氧化铁(其余为杂质,且杂质中不含有铁元素)求:(1)氧化铁中各元素的质量比;(2) 氧化铁中铁元素的质量分数;
(3)若赤铁矿中含有氧化铁质量分数为80%,则200g该铁矿石中含有多少克铁元素?
富含淀粉的谷物、甘薯等可以酿酒.在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精.香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的.家庭一般制作酒酿的简单流程图如下(注:有机反应化学方程式可用箭号表示):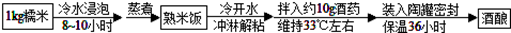
(1)配平化学方程式:(C6H10O5)n(淀粉)+________H2O nC6H12O6(葡萄糖).
nC6H12O6(葡萄糖).
(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C6H12O4(葡萄糖) 2________(乳酸).
2________(乳酸).
(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C2H5OH)和二氧化碳,写出该反应的化学方程式:________________________________________________.
(4)若用1kg大米酿米酒,假设其中有0.81kg的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10%的米酒________kg.
[提示]由淀粉转化为酒精的关系式为(C6H10O5)n~2nC2H5OH.
某同学欲测定草木灰中碳酸钾的含量,称取69g试样于烧杯中,加入29.2g稀盐酸恰好完全反应,反应后,称得混合物的总质量为93.8g(忽略二氧化碳的溶解对质量的影响).请计算:
(1)反应过程中产生的二氧化碳质量为________g.
(2)该草木灰试样中碳酸钾的质量分数.
小青在实验室发现一瓶长期敞口放置的浓盐酸,为方便以后使用,他对其浓度进行了测定.取10g该盐酸于烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)测定溶液的pH,得到的数据如下:
| 加入氢氧化钠的体积/mL |
0 |
1.0 |
8.0 |
9.5 |
10.5 |
12.0 |
16.5 |
| 烧杯中溶液的pH |
1.0 |
1.3 |
2.0 |
3.9 |
9.9 |
11.9 |
12.8 |
(1)请你绘制出烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系图.
(2)请根据下图找出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积数,并据此计算该瓶盐酸的溶质质量分数.(氢氧化钠溶液的密度按1.0g/mL计算)
硫酸铜溶液对过氧化氢(H2O2)的分解有催化作用.取8.5%的过氧化氢溶液40g倒入小烧杯中,向其中加入20%的硫酸铜溶液6.6g,使过氧化氢完全分解.计算:
(1)产生氧气的质量.
(2)反应后所得溶液中硫酸铜的质量分数.
汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2克/厘米3.若要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630克.求:
(1)630克稀硫酸的体积是多少毫升?
(2)需要浓硫酸多少克?