根据下图海水综合利用的工业流程图,判断下列说法不正确的是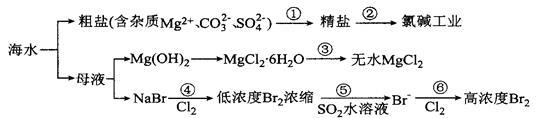
已知:MgCl2·6H2O受热生成Mg(OH) Cl和HC1气体等。
| A.过程①的提纯是化学过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O直接灼烧得不到MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
下列说法不正确的是
| A.加热可鉴别碳酸氢钠与碳酸钠 |
| B.焰色反应可鉴别钾盐和钠盐 |
| C.用水可鉴别氢氧化镁和氢氧化铝固体 |
| D.KSCN溶液可鉴别Fe3+与Fe2+ |
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是
| A.无水硫酸铜 | B.硫酸亚铁 | C.食盐 | D.生石灰 |
已知氨气极易溶于水,其水溶液呈碱性,某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4的工艺流程如下:
下列推断合理的是
| A.甲为CO2,乙为NH3 |
| B.由滤液提纯(NH4)2SO4过程中的实验操作为萃取 |
| C.CO2可被循环使用 |
| D.上述过程中涉及到的反应全部是氧化还原反应 |
向H2SO4、CuCl2混合溶液中投入足量的铁粉,经充分反应后,过滤、洗涤、干燥、称重,知所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42﹣)与c(Cl﹣)之比
| A.1:2 | B.1:7 | C.7:1 | D.1:14 |
2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖。钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O == CO2+Pd↓+2HCl。下列说法正确的是
| A.题述反应中PdCl2被氧化 |
| B.生成约22.4 L CO2时,转移的电子数为2 mol |
| C.上述反应中PdCl2是氧化剂,CO2是氧化产物 |
| D.CO气体只有在高温下才能表现还原性 |