本题有两部分
I:软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4·H2O,反应的化学方程式为:MnO2+SO2=MnSO4
(1)质量为17.4g纯净MnO2最多能氧化____________L(标准状况)SO2。
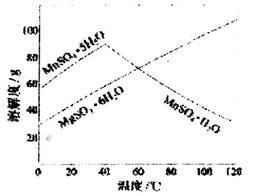
(2)上述反应制得的溶液,调节pH值到5~7的范围,以除去Fe3+、 Al3+(使其浓度小于l×10-6mol·L-1),然后从得到的MnSO4和 MgSO4混合溶液中结晶MnSO4·H2O晶体,下图可以看出,需控制结晶温度在_______以上。
II:以磷石膏(主要成分CaSO4,杂质SiO2、A12O3等)为原料可制备轻质CaCO3。

(1)匀速向浆料中通入CO2,浆料清液的pH和c(SO42-)随时间变化见下图。清液pH>11时CaSO4转化的离子方程式_______________________

(2)当清液pH接近6.5时,过滤并洗涤固体。滤液中物质的量浓度最大的两种阴离子为SO42-和_______(填化学式);检验洗涤是否完全的方法是____________。
(3)磷石膏若用氢氧化钠溶液溶解,发生反应的有关离子方程式为:
_________________________________ 、____________________________________
一定体积的二氧化碳被体积为V mL的氢氧化钠溶液完全吸收后,经检验发现溶液中的氢氧化钠已经完全反应。将上述反应后的液体分为两等份。
(1)甲同学向其中的一份加入足量的澄清石灰水,得到沉淀的质量为M g。据此,能否确定最初通入的CO2在标准状况下的体积?如果能,请列出计算式;如果不能,请在下面的横线上填写“不能”。
答:_________________________________________________________________________。
能否据此确定氢氧化钠溶液的浓度?如果能,请列出计算式;如果不能,请在下面的横线上填写“不能”。
答:___________________________________________________________________________。
(2)乙同学向第二份溶液中滴加足量的CaCl2溶液,最终得到干燥沉淀N g。据此判断M与N的相对大小关系是:__________________________________________________。
大气中二氧化碳含量增多引起温室效应,使地球表面温度升高,有人认为地球上部分地区干旱就是温室效应的后果。
(1)空气中二氧化碳的主要来源是____________________________________________。
(2)自然界消耗二氧化碳的主要过程有__________________________________________。
(3)你认为要防止温室效应的发生,可采取的措施是什么?
(4)二氧化碳是一种重要的无机物,请列举二氧化碳在工业生产和社会生活方面的重要用途。(不少于4种)
下图为一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线。试完成下列问题: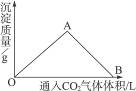
OA段曲线和AB段曲线所表示的反应方程式是
OA:_________________________________________________________________________;
AB:_________________________________________________________________________。
A点时已参加反应的CO2和Ca(OH)2的物质的量之比为_______________。
B处溶液中存在的浓度较大的两种离子是_____________和_____________(填离子符号)。
将B处生成的溶液煮沸,可见到的现象是______________________________。
(5分)已知A是灰黑色硬而脆的固体,B是气态物质,根据下图所示关系确定各字母所代表的物质的名称:
A________,B________,C________,D________,E________。
由淀粉和其他无机原料,合成环状化合物H: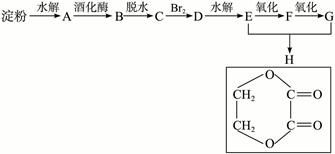
写出下列物质的结构简式:
| A.________________, | B._________________, | C._________________, | D._________________,E._________________,F._________________,G._________________。 |