CuCl是难溶于水的白色固体,是一种重要的催化剂。工业上,由孔雀石(主要成分Cu(OH)2·CuCO3,含FeS、FeO和SiO2杂质)制备CuCl的某流程如下: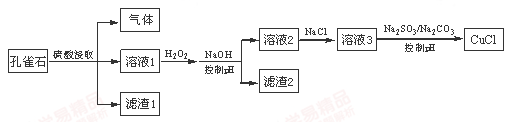
下列说法不正确的是
| A.H2O2将溶液1中Fe2+氧化为Fe3+,再通过控制pH转化为Fe(OH)3除去 |
| B.SO32-将溶液3中的Cu2+还原,反应得到CuCl |
| C.CO32-作用是控制溶液pH,促使CuCl沉淀的生成 |
| D.若改变试剂加入顺序,将溶液3缓慢加入到含大量SO32-/CO32-的溶液中,同样可制取CuCl |
有a、b、c、d四种元素,a、b为同周期元素,c、d为同族元素。已知a的阳离子和d的阴离子具有相同的电子层结构。b的阴离子和c的阴离子电子层结构相同。且c离子的电荷数大于b离子。则下列说法正确的是( )
①原子序数d>b>c>a②原子序数d<a<c<b③原子序数d<a<b<c④离子半径b>c>d>a⑤离子半径b>c>a>d⑥离子半径c>b>d>a
| A.③④ | B.②⑥ | C.①⑤ | D.②④ |
元素R的气态氢化物的化学式为H2R,这种气态氢化物的相对分子质量与R的最高价氧化物的相对分子质量比为1∶2.35,下列对元素R的描述正确的是( )
| A.元素R能与氧组成RO2化合物 |
| B.化合物RO2在反应中既可作氧化剂也可作还原剂,其化合物不稳定 |
| C.化合物H2R不能燃烧,也不易分解 |
| D.元素R是一种两性元素 |
如果发现了原子序数为116的元素,对它的描述正确的是( )
①位于第7周期②是非金属元素③最外电子层含有6个电子④没有放射性⑤属于氧族元素⑥属于卤素
| A.①③⑤ | B.①③⑥ | C.②④⑥ | D.②③⑤ |
短周期元素X、Y可形成化合物X2Y3,若已知Y的原子序数为m,则X的原子序数不可能是()
| A.m+5 | B.m-13 | C.m+6 | D.m-3 |
下列排列顺序不正确的是( )
| A.微粒半径 Na+>K+>Cl->S2- |
| B.稳定性 HI>HBr>HCl>HF |
| C.酸性 HClO4>H2SO4>H3PO4>H2SiO3 |
| D.碱性 KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |