已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 452 kJ/mol
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列说法正确的是
| A.H2(g)的燃烧热ΔH=-571.6 kJ/mol |
B. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)===BaSO4(s)+H2O(l) ΔH=-57.3 kJ/mol Ba(OH)2(aq)===BaSO4(s)+H2O(l) ΔH=-57.3 kJ/mol |
| C.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| D.3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=+135.9 kJ/mol |
下面是几种常见的化学电源示意图,有关说法不正确的是
| A.上述电池分别属于一次电池、二次电池和燃料电池 |
| B.干电池在长时间使用后,锌筒被破坏 |
| C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g |
| D.氢氧燃料电池是一种具有应用前景的绿色电源 |
1L某溶液中含有的离子如下表:
| 离子 |
Cu2+ |
Al3+ |
NO3- |
Cl- |
| 物质的量浓度(mol/L) |
1 |
1 |
a |
1 |
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是
A.电解后溶液pH=0 B.a=3
C.阳极生成1.5mol Cl2 D.阴极析出的金属是铜与铝
下列说法正确的是
A.氢气的燃烧热为△H=-285.5k•Jmol-1,则电解水的热化学方程式为2H2O(l) 2H2(g)+O2(g) △H=+285.5k•Jmol-1 2H2(g)+O2(g) △H=+285.5k•Jmol-1 |
B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量。则Fe(s)+S(s)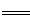 FeS(s) △H=-95.6kJ•mol-1 FeS(s) △H=-95.6kJ•mol-1 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6k•Jmol-1 2NH3(g) △H=-38.6k•Jmol-1 |
| D.相同条件下,在两个相同的恒容密闭容器中,1molN2和3molH2反应放出的热量与2molN2和3molH2反应放出的热量一样多 |
某实验过程如图所示,则图③试管中的现象是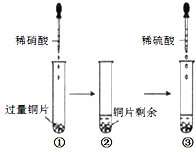
| A.铜片溶解,产生无色气体,该气体遇空气变为红棕色 |
| B.铜片溶解,产生无色气体,该气体遇到空气不变色 |
| C.铜片溶解,放出红棕色有刺激性气味的气体 |
| D.无明显现象,因稀硫酸不与铜反应 |
实验是化学研究的基础,下图装置或操作正确的是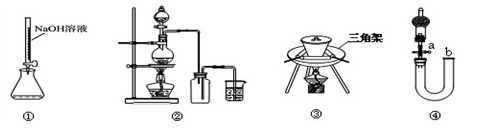
| A.用装置①量取15.00mL的NaOH溶液 |
| B.用装置②制备Cl2 |
| C.用装置③陶瓷坩埚高温煅烧CaCO3固体 |
| D.关闭活塞a,从b处加水,以检查装置④的气密性 |