对于可逆反应mA(g)+nB(s) pC(g)+qD( g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是
pC(g)+qD( g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是
| A.化学方程式中化学计量数:p+q> m+n |
| B.降温可使化学平衡向正反应方向移动 |
| C.使用合适的催化剂可使D%有所增加 |
| D.加入少量的B,正反应速率加快,有利于平衡向正反应方向移动 |
下列离子方程式正确的是( )
| A.乙酸与碳酸钠溶液反应:2H++CO32—== CO2↑+H2O |
| B.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
| C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O →2C6H5OH+CO32— |
D.甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-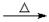 CO32—+2NH4++4Ag↓+6NH3+2H2O CO32—+2NH4++4Ag↓+6NH3+2H2O |
某一溴代烷水解后的产物在红热铜丝催化下,最多可被空气氧化生成4种不同的醛,该一溴代烷的分子式可能是( )
| A.C4H9Br | B.C5H11Br | C.C6H13Br | D.C7H15Br |
某学生做实验后,采用下列方法清洗所有仪器:①用稀HNO3清洗做过银镜反应的试管②用酒精清洗做过碘升华的烧杯③用盐酸清洗长期盛放FeCl3溶液的试剂瓶④用盐酸溶液清洗盛过苯酚的试管。你认为他的操作( )
| A.②不对 | B.③不对 | C.④不对 | D.全部正确 |
下列关于醇和酚的说法中,正确的是( )
| A.含有羟基的化合物一定是醇 |
| B.分子内有苯环和羟基的化合物一定是酚 |
| C.羟基跟链烃基相连时,有机物为醇 |
| D.酚和醇具有相同的官能团,因而具有相同的化学性质 |
下列有机物中,能发生消去反应生成2种烯烃,又能发生水解反应的是( )
| A.1-溴丁烷 | B.2-甲基-3-氯戊烷 |
| C.2,2-二甲基-1-氯丁烷 | D.1,3-二氯苯 |