相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:X2 (g)+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0) |
下列叙述不正确的是( )
A、容器①中达到平衡时,Y2的转化率为50%
B、Q="27.78" kJ
C、相同温度下;起始时向容器中充入1.0 X2 mol 、3.0 mol Y2和2 mol XY3;反应达到平衡前v(正)>v(逆)
D、容器①、②中反应的平衡常数相等,K=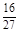
已知在酸性条件下能发生下列反应:Cu+→Cu + Cu2+(未配平)。NH4CuSO3与足量的10 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是()
| A.NH4CuSO3中硫元素被氧化 | B.该反应显示硫酸具有酸性 |
| C.刺激性气味的气体是氨气 | D.反应中硫酸作氧化剂 |
铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg,那么一个铅笔字含有的碳原子个数约为()
| A.2.5×1019 | B.2.5×1022 | C.5×1019 | D.5×1022 |
化学与生活、社会密切相关。下列说法正确的是()
| A.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂 |
| B.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化和消毒 |
| C.广州亚运会上燃放的绚丽焰火是某些金属元素魅力的展现 |
| D.外加直流电源,将钢铁设备作为阳极可有效进行保护 |
下列化学反应的离子方程式,书写不正确的是
| A.硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-= BaSO4↓ |
B.向氯化铝溶液中加入过量氢氧化钠溶液:Al3++4OH—=AlO +2H2O +2H2O |
| C.氯化亚铁溶液中通入少量氯气:Cl2+ 2Fe2+=2Fe3+ +2Cl— |
| D.碳酸钙加入稀盐酸: CaCO3+2H+=Ca2+ +CO2↑+H2O |
下列叙述中,正确的是
| A.0.3 mol/L的Na2SO4溶液中含有Na+ 和SO42-的总物质的量为0.9 mol |
| B.当1 L水吸收标准状况下的22.4 L氯化氢时所得盐酸的浓度是1 mol/L |
| C.在K2SO4和NaCl的中性混合水溶液中,如果Na+ 和SO42-的物质的量相等,则K+ 和Cl—的物质的量浓度一定相同 |
| D.10 ℃时,0.35 mol/L的KCl饱和溶液100 mL蒸发掉5 g水,恢复到10 ℃时,它的物质的量浓度仍为0.35 mol/L |