向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| |
操作 |
现象 |
结论 |
| A |
滴加稀NaOH溶液,将红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无NH4+ |
| B |
向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X 中一定含有SO42- |
| C |
滴加氯水和CCl4,振荡、静置 |
下层溶液显紫色 |
原溶液中有I- |
| D |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
原溶液中有Na+、无K+ |
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断
| A.R一定是第四周期元素 |
| B.R一定是ⅣA族元素 |
| C.R的气态氢化物比同族其他元素气态氢化物稳定 |
| D.R气态氢化物化学式为H2R |
下列关于下图所示原电池装置的叙述中,正确的是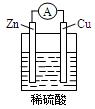
| A.铜片是负极 | B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
下列各组中属于同位素关系的是
A.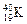 与 与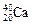 |
B.T2O与H2O | C.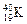 与 与 |
D.金刚石与石墨 |
在铁粉和铜粉的均匀混合物中加入某浓度的硝酸,充分反应,硝酸的还原产物只有NO。当加入硝酸10 mL时,剩余金属1.8 g,生成气体0.224 L;再增加硝酸10mL时,剩余金属0.96 g,又有0.224 L气体生成;继续增加硝酸10 mL时,金属全部溶解,又有0.224L气体生成(以上体积均换算为标准状况下)。下列说法不正确的是()
| A.所加入硝酸的浓度是4 mol/L |
| B.加入硝酸10 mL时,剩余金属为铁和铜 |
| C.共加入硝酸20 mL时,剩余金属只有铜 |
| D.如果在金属混合物中共加入硝酸40 mL时,生成的NO仍是0.672 L(标准状况) |
用酸性氢氧燃料电池电解苦卤水(含Cl —、Br—、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中,正确的是()
—、Br—、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中,正确的是()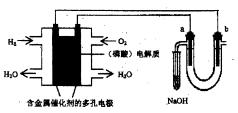
| A.电池工作时,正极反应式为: O2 +2H2O+4e—==4OH |
| B.电解—段时间后,在b电极周围有白色沉淀生成 |
| C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D.当电池中消耗0.02g H2时,b极周围会产生0.224L H2 |