NA为阿伏伽德罗常数的值。下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.1L0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
C.5NH4NO3  2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA |
| D.室温下,l L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.l NA |
在相同的条件下,一定量的氢气在氧气中充分燃烧并放出热量。若生成液态水放出的热量为Q1 kJ;若生成气态水放出的热量为Q2 kJ。那么Q1与Q2之间的关系
| A.Q1>Q2 | B.Q1<Q2 | C.Q1=Q2 | D.不能确定 |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说中一定正确的是
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| C.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| D.有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
将表面被氧化的铜片和铁片,同时加入足量稀盐酸中,除尽氧化膜。再经充分反应后,溶液中一定含有的金属离子是
| A.Fe2+ | B.Fe2+和Cu2+ | C.Fe3+和Cu2+ | D.Fe2+和Fe3+ |
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g),甲醇生成量与时间的关系如图所示。下列有关说法正确的是.
CH3OH(g),甲醇生成量与时间的关系如图所示。下列有关说法正确的是.
| A.在300 ℃条件下,t1时刻该反应达到化学平衡 |
| B.在500 ℃条件下,从反应开始到平衡,氢气的平均反应速率v(H2)为nB/(3t1) mol/L |
| C.在其他条件不变的情况下,将处于E点的体系体积压缩到原来的1/2,则氢气的浓度减小 |
| D.由图像说明该反应的正反应为放热反应 |
在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气)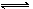 xC(气)+yD(气)达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则x、y的值分别为
xC(气)+yD(气)达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则x、y的值分别为
A.x=3 y=1 B.x=4 y="1" C.x=5 y =1 D.x=8 y=2