氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
请回答下列有关含氮物质的问题:
(1)右图是1molNO2和1molCO反应生成CO2 和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式_____________________________________;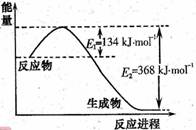
恒温恒容条件下,不能说明该反应已达到平衡状态的是___(填序号)。
| A.容器内混合气体颜色不再变化 |
| B.容器内的压强保持不变 |
| C.v逆(NO2)=v正(NO) |
| D.容器内混合气体密度保持不变 |
(2)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g) 2NO(g) ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。
2NO(g) ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。
该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol/L、4.0×10-2 mol/L和3.0×10-3 mol/L,此时反应_______(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”)。
(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。总电池反应为N2H4+O2 = N2+2H2O。该电池放电时,负极的电极反应式是_________。
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式_____________________________________。
在一容积为2L且容积不变的密闭容器中加入适量碳粉和0.2molH2O。在800℃条件下,经20s后达到如下化学平衡:C(s) +H2O(g)  CO(g) + H2(g);△H=" -Q" kJ·mol-1(Q>0)。已知达到平衡时,CO为0.12mol。试回答:
CO(g) + H2(g);△H=" -Q" kJ·mol-1(Q>0)。已知达到平衡时,CO为0.12mol。试回答:
(1)其他条件不变,若加入少量碳,则平衡移动情况是:________________;
(2)若用υ(H2O)表示该反应前20s内的平均速率,则υ(H2O)=" ________________" ;
(3)若向上述平衡的混合物中再充入0.08mol H2,在相同条件下达到新的平衡,此时CO的物质的量为________________mol。
(1)工业上Al2Te3可用来制备H2Te,完成下列化学方程式并配平:
()Al2Te3+()
()Al( OH)3↓+()H2Te↑
OH)3↓+()H2Te↑
(2)在101kPa时,4.0g硫粉在氧气中完全燃烧生成SO2,放出37kJ的热量,则硫燃烧的热化学方程式为。
(12分)(1)1 mol分子组成为C3H8O的液体有机物A,与足量的金属钠作用,可生成11.2 L氢气(标准状况),则A分子中必有一个____________基,若此基在碳链的一端,则A的结构简式为________________.
(2)A与浓硫酸共热,分子内脱去1分子水,生成B.B的结构简式为____________.
B通入溴水能发生反应,生成C.C的结构简式为___________.A在有铜作催化剂时,与氧气一起加热,发生氧化反应,生成D.D的结构简式为________.
(3)写出下列指定反应的化学方程式:
①A―→B__________________________________________________;
②A―→D____________________________________________________.
根据下面的反应路线及所给信息填空
(1)A的结构简式是
(2)①的反应类型是。③的反应类型是。
(3)反应④的化学方程式是。
( 6分)(1)键线式 表示的分子式;名称是。
表示的分子式;名称是。
(2) 中有氧官能团的名称为
中有氧官能团的名称为