常温下,下列溶液可能大量共存的离子组是( )

| A.含有大量S2—的溶液:Na+、C1O—、C1—、CO32— |
| B.含有大量Fe3+的溶液:K+、Na+、A1O2—、SO42— |
| C.能使pH试纸变红的溶液:NH4+、Na+、NO3—、HCO3— |
| D.水电离产生的c(H+)=1×10—12mol·L—1的溶液:Mg2+、SO42—、NO3—、C1— |
下列物质中,属于电解质的是
A.Na CO CO 溶液 溶液 |
B.NaCl | C.蔗糖 | D.Cu |
根据气象台报道,近年每到春季,沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的
| A.胶体 | B.悬浊液 | C.乳浊液 | D.溶液 |
经测定某溶液中只有Na+、CH3COO-、H+、OH-四种离子,且其浓度大小的排列顺序为:c (Na+)>c(CH3COO-)>c(OH-)>c(H+),下列有关说法正确的是
| A.该溶液由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由0.1 mol·L-1的CH3COOH溶液与0.1 mol·L-1的CH3COONa溶液等体积混合而成 |
| C.在上述溶液中加入适量CH3COOH,可能使溶液中离子浓度大小改变为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.在上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为:c(CH3COO-)=c(Na+)>c(OH-)=c(H+) |
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是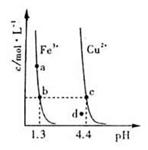
| A.Kap[Fe(OH)3]<Kap[Cu(OH)2] |
| B.加适量NH4Cl固体可使溶液由a点变到b点 |
| C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
| D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 |
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS (s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
| A.-1780kJ/mol | B.-1220 kJ/mol |
| C.-450 kJ/mol | D.+430 kJ/mol |