等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应,若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为
| A.1:2:3 | B.1:6:9 | C.1:3:3 | D.1:3:6 |
下列有关有机物  的命名正确的是
的命名正确的是
| A.3—甲基—1—丁烯 | B.2—乙基—1—丙烯 |
| C.3—甲基—3—丁烯 | D.2—甲基—1—丁烯 |
下列各组液体混合物,能用分液漏斗分离的是
| A.乙酸和乙醛 | B.乙醇和水 |
| C.苯和苯酚 | D.溴乙烷和水 |
下列化学用语表达正确的是
A.乙酸的分子比例模型图: |
B.聚丙烯结构简式: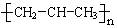 |
| C.醛基的结构简式:—COH | D.乙烯的结构简式:CH2CH2 |
生活离不开化学。下列对生活中各种物质的认识不正确的是
| A.酒精可用于消毒杀菌 |
| B.液化石油气的主要成分属于烃类 |
| C.塑料、油脂、橡胶均属于高分子化合物 |
| D.普通肥皂的主要成分是高级脂肪酸钠盐 |
对于常温下pH为1的硝酸溶液,下列叙述正确的是

A.该溶液1mL稀释至100mL后,pH等于3 |
B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 |
C.该溶液中硝酸电离出的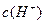 与水电离出的 与水电离出的 之比值为 之比值为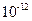  |
D.该溶液中水电离出的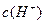 是pH为3的硝酸中水电离出的 是pH为3的硝酸中水电离出的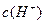 的100倍 的100倍 |