三聚氰胺又名蛋白精[分子式:C3N3(NH2)3,相对分子质量:126]是一种低毒性化工产品,婴幼儿大量摄入可引起泌尿系统疾患,下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.2.52 g三聚氰胺含氮原子数目为0.12NA |
| B.标准状况下1 mol的三聚氰胺的体积为22.4 L |
| C.三聚氰胺含氮量约为10% |
| D.三聚氰胺的摩尔质量为126 |
为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是
| 物质 |
试剂 |
分离方法 |
|
| ① |
硝酸钾(氯化钠) |
蒸馏水 |
降温结晶 |
| ② |
二氧化碳(氯化氢) |
饱和碳酸钠溶液 |
洗气 |
| ③ |
乙醇(水) |
生石灰 |
蒸馏 |
| ④ |
苯(苯酚) |
浓溴水 |
分液 |
| A.①② | B.①④ | C.①③ | D.③④ |
以下实验能获得成功的是
| A.用醋酸钠晶体和碱石灰共热制甲烷 |
| B.将铁屑、溴水、苯混合制溴苯 |
| C.在苯酚溶液中滴人少量稀溴水出现白色沉淀 |
| D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
下列各组离子能在指定溶液中大量共存的是
| A.在能使石蕊试纸变蓝色的溶液中:Na+、SO32ˉ、S2ˉ、SO42ˉ |
| B.由水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Clˉ、CO32ˉ、NH4+、NO3ˉ |
| C.在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3ˉ |
| D.pH=2的溶液中:Na+、SO42ˉ、NO3ˉ、AlO2ˉ |
共价化合物含C、H、N三种元素。分子内有四个N原子,成四面体;每两个N原子之间都含有1个C原子。又知分子中无C一C键和C=C键,该化合物的分子式
A.C3H8N4 B.C6H12N4C.C6H10N4 D.C4H8N4
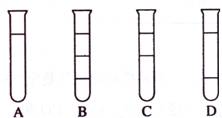
将等体积的苯、汽油和水在试管中充分混合后静置。下列图示现象正确的是: