下列条件下,两瓶气体所含的原子数一定相等的是
①同质量不同密度的CO和N2
②同温同体积的H2和Cl2
③同体积同密度的O2和O3
④同压同体积的N2O和CO2
| A.①③ | B.①② |
| C.②④ | D.③④ |
右图表示反应N2(g)+3H2(g) 2NH3(g)△H<0,在某一时间段中反应速率与反应过程的曲线关系图。下列说法正确的是
2NH3(g)△H<0,在某一时间段中反应速率与反应过程的曲线关系图。下列说法正确的是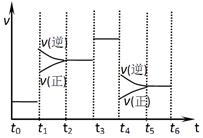
| A.氨气的体积分数最高的一段时间为t5~t6 |
| B.t2~t3和t3~t4时间段氨气的体积分数相等 |
| C.t1时刻改变的条件是降低温度 |
| D.t4~t5时间段平衡向正反应方向移动 |
室温下,水的电离达到平衡:H2O H++OH-。下列叙述正确的是
H++OH-。下列叙述正确的是
| A.将水加热,平衡向正向移动,Kw不变 |
| B.向水中加入少量NaOH固体,平衡向逆向移动,c(OH-)增大 |
| C.新制氯水久置后,水的电离平衡向正向移动,c(OH-)增大 |
| D.向水中加入少量CH3COONa固体,平衡向正向移动,Kw增大 |
下列物质属于强电解质的是
| A.NH3·H2O | B.H2O | C.CH3COOH | D.醋酸铵 |
改变反应容器体积使压强变化,但不会使下列化学反应的平衡发生移动的是
A.Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) 2Fe(s)+3CO2(g) |
B.3H2(g)+N2(g) 2NH3(g) 2NH3(g) |
C.2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
D.C(s)+CO2(g) 2CO(g) 2CO(g) |
已知H2+I2 2HI△H<0。有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
2HI△H<0。有相同容积的定容密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
| A.甲、乙提高相同温度 |
| B.甲中加入0.1 molHe,乙不改变 |
| C.甲降低温度,乙不变 |
| D.甲增加0.1 molH2,乙增加0.1 mol I2 |